Biochemický slovník
Biochemický slovník
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
F |
|---|
FADobecně užívaná zkratka pro flavinadenindinukleotid, kofaktor, jehož strukturní základ tvoří 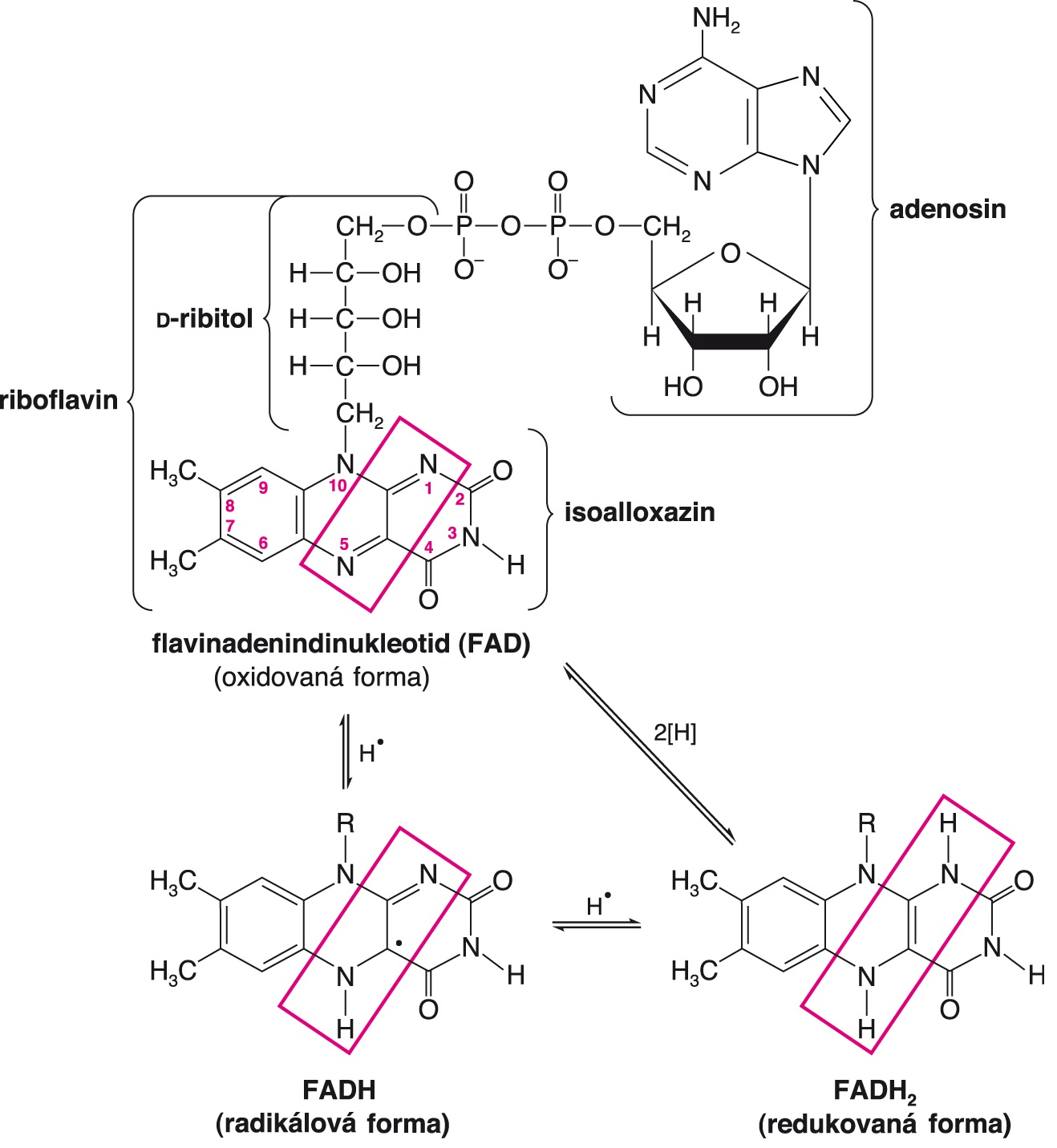 heterocyklická isoalloxazinová struktura. V oxidované formě je žlutý, redukcí (přijetím dvou atomů vodíku) přechází na bezbarvou formu. Isoalloxazin připojený na cukerný alkohol ribitol je vitamin B2 - riboflavin. FAD je prostetickou skupinou mnoha enzymů třídy oxidoreduktas, a to zejména oxidas (např. glukosaoxidasa), ale i dehydrogenas, které katalyzují odtržení dvou atomů vodíku z alkanového řetězce za vzniku dvojné vazby (např. sukcinátdehydrogenasa, EC 1.3.5.1, v citrátovém cyklu nebo acyl-CoA-dehydrogenasa, EC 1.3.8.1; EC 1.3.8.8 v β-oxidaci mastných kyselin). Podobnou funkci zastává i flavinmononukleotid (FMN, neobsahuje adenosinfosfát), významný zejména jako prostetická skupina kotveného komplexu I v dýchacím řetězci. Za výzkum flavonoidů a vitaminu B2 získal roku 1937 P. Karrer Nobelovu cenu. heterocyklická isoalloxazinová struktura. V oxidované formě je žlutý, redukcí (přijetím dvou atomů vodíku) přechází na bezbarvou formu. Isoalloxazin připojený na cukerný alkohol ribitol je vitamin B2 - riboflavin. FAD je prostetickou skupinou mnoha enzymů třídy oxidoreduktas, a to zejména oxidas (např. glukosaoxidasa), ale i dehydrogenas, které katalyzují odtržení dvou atomů vodíku z alkanového řetězce za vzniku dvojné vazby (např. sukcinátdehydrogenasa, EC 1.3.5.1, v citrátovém cyklu nebo acyl-CoA-dehydrogenasa, EC 1.3.8.1; EC 1.3.8.8 v β-oxidaci mastných kyselin). Podobnou funkci zastává i flavinmononukleotid (FMN, neobsahuje adenosinfosfát), významný zejména jako prostetická skupina kotveného komplexu I v dýchacím řetězci. Za výzkum flavonoidů a vitaminu B2 získal roku 1937 P. Karrer Nobelovu cenu. | |
fagocytózaz řeckého fagein = pojídání; angl. phagocytosis, endocytický proces, jímž buňky (u savců zejména určité druhy bílých krvinek – makrofágy) pohlcují a rozkládají pevné částice, obvykle jinou buňku nebo její část. Tímto způsobem jsou z cirkulace odstraňovány
bakterie, částice pocházející z nekrotické (odumírající) tkáně, staré erythrocyty apod. Fagocytózou vzniká organela zvaná fagosom, která po spojení s primárním lysosomem vytváří sekundární lysosom, v němž jsou pohlcené makromolekuly hydrolyticky rozloženy. | |
faktorangl. factor, pojem užívaný v
biochemii pro látku, o jejímž mechanismu působení v danou chvíli nejsou jasné informace, je však zjevné, že pro daný děj je jeho přítomnost zásadní. Často pak tento název určité látky přežívá i v době, kdy je mechanismus jejího působení objasněn. Napřiklad v molekulové genetice se hovoří o bílkovinných faktorech iniciačních, elongačních a uvolňovacích, o terminačním ρ-faktoru, o σ-faktoru (též σ-podjednotce) jakožto součásti RNA-polymerasy; významné jsou též výživové esenciální faktory a koagulační faktory. | |
faktory koagulačníangl. clotting nebo coagulation factors, molekulové komponenty, které se účastní komplexního procesu
krevní koagulace. Mezi tyto faktory jsou (nebo byly) řazeny nejen enzymy a ostatní proteiny koagulační kaskády, ale také fibrinogen, vitamin K (fyllochinon) a vápenaté ionty. | |
faktory výživové esenciálníangl. essential food factors, složky potravy (výživy), které jsou pro určitý
heterotrofní organismus nezbytné. Řadíme sem především esenciální aminokyseliny a nenasycené mastné kyseliny, vitaminy a minerální látky (zejména ionty kovů). U mikroorganismů, které nejsou plně autotrofní (nazývají se auxotrofní), se těmto faktorům říká růstové faktory; mohou to být některé vitaminy a peptidy, ale také báze nukleových kyselin. | |
Fenn John Bennett
| |
fenotypangl. phenotype, zjevné nebo nějakým způsobem objektivně měřitelné charakteristiky organismu, které jsou důsledkem interakce jeho genetické výbavy (viz genotyp) s prostředím, v němž probíhá jeho individuální vývoj. | |
fenylalaninPhe nebo F, angl. phenylalanine, aromatická proteinogenní esenciální 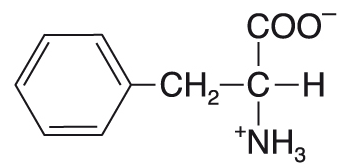 ketogenní aminokyselina. Postranní řetězec je výrazně hydrofobní. Prvním krokem jejího odbourávání je enzymová hydroxylace, jíž vzniká tyrosin (viz fenylketonurie). Fenylalanin se užívá k výrobě voňavek a k syntéze nízkokalorického umělého peptidového sladidla aspartamu (L-Asp-L-Phe-methylester). ketogenní aminokyselina. Postranní řetězec je výrazně hydrofobní. Prvním krokem jejího odbourávání je enzymová hydroxylace, jíž vzniká tyrosin (viz fenylketonurie). Fenylalanin se užívá k výrobě voňavek a k syntéze nízkokalorického umělého peptidového sladidla aspartamu (L-Asp-L-Phe-methylester). | |
fenylketonurieangl. phenylketonuria, dědičné onemocnění, způsobené nedostatečnou aktivitou enzymu katalyzujícího přeměnu
fenylalaninu na tyrosin (fenylalanin-4-monooxygenasa, též fenylalaninhydroxylasa, EC 1.14.16.1). Projevuje se vylučováním fenylpyruvátu močí. V našich končinách patří k nejčastěji se vyskytujícím enzymopatiím (1z 9 000 živě narozených dětí); proto je od roku 1975 každý novorozenec testován na toto onemocnění. Choroba je doprovázena psychickými poruchami. Patologické důsledky lze redukovat pečlivou dietou spočívající v přísné regulaci příjmu fenylalaninu, resp. bílkovin. | |
fermentangl. ferment, starší, dnes již velmi málo používané označení pro
enzym; termín zůstal obsažen v pojmu fermentace. | |
fermentaceangl. fermentation, komplexní pojem užívaný v různých souvislostech:
| |
fermentace aerobníangl. aerobic fermentation, procesy, při nichž ve
fermentoru působí mikroorganismy za aerobních podmínek (např. aerobní stupeň čištění odpadních vod, fermentační výroba kyseliny citronové - srov. fermentace nepravá); nepříliš vhodný, avšak v praxi používaný termín. | |
fermentace nepravátéž nepravé kvašení, angl. false fermentation, aerobní metabolický typ některých chemoorganotrofů, u nichž se výchozí organický substrát neoxiduje až na
CO2 a H2O, ale konečným produktem je organická látka (obvykle organická kyselina, srov. aerobní fermentace). Průmyslově se využívá zejména octové kvašení (bakteriální oxidace ethanolu na octovou kyselinu), oxidace glukosy na glukonovou kyselinu a přeměna sacharidů nebo n-alkanů na citronovou kyselinu. | |
ferredoxinyangl. ferredoxins, skupina
peptidů (kolem 55 aminokyselin) přenášejících elektrony od jednoho enzymového systému ke druhému; samy však nevykazují enzymovou aktivitu. Obsahují nehemově vázané železo (viz FeS-proteiny). Uplatňují se především ve fotosyntéze, jakož i při fixaci atmosférického dusíku a oxidu uhličitého bakteriemi. | |
ferritinangl. ferritin, nejdůležitější bílkovina skladující železo v savčím organismu. Molekula ferritinu tvořená 24 identickými podjednotkami má celkovou molekulovou hmotnost
445 kDa a může skladovat až 4 300 atomů železa (resp. iontů Fe3+). Nachází se především ve slezině, játrech, kostní dřeni a retikulocytech (nezralé erythrocyty). | |
FeS-proteinyangl. FeS-proteins, bílkoviny, které obsahují (nehemově) vázané ionty železa (Fe3+). Železo 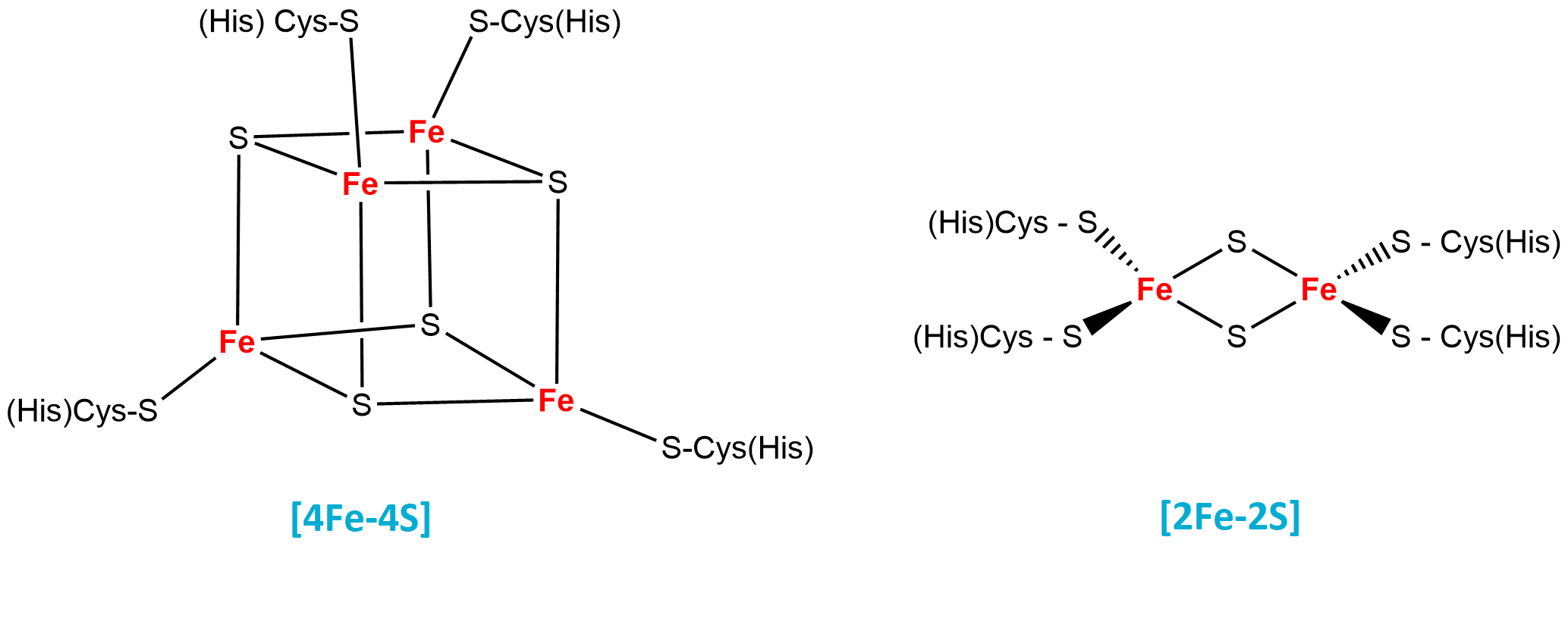 zde obvykle vytváří komplexní struktury se sulfidovými ionty (S2-); celá prostetická skupina je k peptidové části molekuly připojena prostřednictvím postranních řetězců Cys a někdy též His. FeS-proteiny působí jednak jako přenašeče elektronů (viz ferredoxiny), jednak jako enzymy ze třídy oxidoreduktas, které přenášejí elektrony od jednoho substrátu k druhému (transelektronasy, např. některé kotvené komplexy v dýchacím řetězci). Elektrony jsou přenášeny tak, že Fe3+ se dočasně redukuje na Fe2+. zde obvykle vytváří komplexní struktury se sulfidovými ionty (S2-); celá prostetická skupina je k peptidové části molekuly připojena prostřednictvím postranních řetězců Cys a někdy též His. FeS-proteiny působí jednak jako přenašeče elektronů (viz ferredoxiny), jednak jako enzymy ze třídy oxidoreduktas, které přenášejí elektrony od jednoho substrátu k druhému (transelektronasy, např. některé kotvené komplexy v dýchacím řetězci). Elektrony jsou přenášeny tak, že Fe3+ se dočasně redukuje na Fe2+. | |
fibrinangl. fibrin, bílkovinná struktura nerozpustná ve vodě, produkt
koagulace krve. Vzniká z bílkoviny fibrinogenu přítomné v krevní plasmě, a to účinkem enzymu thrombinu za přítomnosti vápenatých iontů. Thrombin odštěpuje z peptidových řetězců fibrinogenu dva páry peptidů, označovaných fibrinopeptidy A a B, a převádí ho tak na aktivní formu - fibrinmonomer; jeho samovolnou polymerací vzniká fibrinové vlákno. Ve vzniklém polymeru se působením specifického enzymu vytvářejí příčné kovalentní vazby mezi postranními řetězci glutamové kyseliny a lysinu, čímž se fibrin stabilizuje. Při poranění cév tak vzniká, s pomocí dalších účastníků tohoto procesu (krevní destičky, erythrocyty), poměrně pevná struktura (krevní sraženina), která zabraňuje dalšímu krvácení. | |
fibrinogenangl. fibrinogen, jedna z největších a nejhojnějších bílkovin
krevní plasmy, je obsažen také v krevních destičkách. Je tvořen dvěma trojicemi polypeptidových řetězců Aα, Bβ a γ, propojených disulfidovými můstky. Symboly Aα a Bβ označují kompletní polypeptidové řetězce s fibrinopeptidy A a B, které se odštěpují thrombinem; tím se molekula fibrinogenu převede na aktivní formu - fibrin, který následně polymeruje a vytváří krevní sraženinu (koagulum). | |
fibrinolýzaangl. fibrinolysis, enzymově řízené rozpouštění
fibrinové sraženiny v organismu. Rozhodující roli zde hraje proteasa plasmin (EC 3.4.21.7), vyskytující se v plasmě ve formě neaktivního zymogenu plasminogenu. Fibrinolýza může být urychlena podáním léčiv ze skupiny fibrinolytik, která zasahují do procesu rozpouštění krevní sraženiny tím, že aktivují (přímo nebo nepřímo) přeměnu plasminogenu na plasmin. Fibrinolytika se podávají např. při infarktu myokardu, plicní embolii a arteriální trombóze. | |
fibroinangl. fibroin, nerozpustná bílkovina ze skupiny
skleroproteinů (fibrilárních bílkovin), tvořící chemickou podstatu vlákna přírodního hedvábí. Jeho dominantním strukturním motivem je β-struktura (skládaný list). | |
fibróza cystickáangl. cystic fibrosis, jedno z nejčastěji se vyskytujících (přibližně 1 z 2 500 jedinců)
vrozených onemocnění. Je vyvoláno defektním genem pro membránovou bílkovinu, která zajišťuje transport chloridových iontů; bylo identifikováno přes 800 mutací. Projevuje se zejména tvorbou nadbytečného množství hlenu v plicích, ale také poruchou funkcí dalších orgánů (slinivky břišní, střeva atd.). Onemocnění je léčitelné, ne však vyléčitelné; neléčené onemocnění bývá smrtelné. | |
filamenta intermediárnítéž střední filamenta, angl. intermediate filaments, jedna z komponent
cytoskeletu tvořená bílkovinnými vlákny o průměru 10 až 15 nm. Jsou přítomna v místech, kde je buňka vystavena mechanickému namáhání; jsou zodpovědná za mechanickou stabilitu buněk a tkání. Například kožní buňky vyšších živočichů obsahují síť středních filament tvořených proteinem keratinem; dalšími složkami těchto struktur bývají vimentin a desmin. Na rozdíl od ostatních složek cytoskeletu se proteiny tvořící střední filamenta velmi liší velikostí a složením jak mezi různými typy buněk, tak mezi odpovídajícími si typy buněk v různých organismech. | |
Fire Andrew Zachary
| |
Fischer Edmond Henri
| |
Fischer Hans
| |
Fischer Herman Emil
| |
Fleming Alexander
| |
flipasyangl. flipases nebo flippases, integrální membránové enzymy (EC 7.5.2.6 a EC 7.6.2.1), zajišťující primární aktivní transport (štěpí ATP) polárních lipidů (zejména fosfolipidů) z extracelulárního prostoru do cytosolu, čímž umožňují nesymetrické rozložení těchto amfifilních molekul v membránách. Pohyb opačným směrem zprostředkují flopasy, které však doposud nebyly zařazeny do enzymového katalogu. | |
Florey Howard Walter
| |
fluidita membránytéž tekutost, angl. membrane fluidity, jedna ze základních vlastností biologické membrány, vyplývající ze schopnosti molekul polárních lipidů v rámci jednotlivých vrstev navzájem měnit své pozice. Chovají se tedy jako molekuly v kapalině; hovoříme zde o dvojrozměrné kapalině. Fluidita membrány závisí na složení membrány a také na teplotě; pod určitou teplotou, zvanou teplota fázového přechodu, membrána přestává být fluidní (ztuhne) a nemůže pak vykonávat své biologické funkce, především transport látek a přenos signálu. Viz lipidová dvojvrstva. | |
FMNzkr. flavinadeninmononukleotid, angl. flavin adenine mononucleotide, viz FAD. | |
fokusace isoelektrickázkr. IEF, angl. isoelectric focusing, separační
elektromigrační metoda, pomocí níž lze rozdělit bílkoviny podle jejich isoelektrických bodů. Při této metodě se nejdříve vytvoří na nosiči (v polyakrylamidovém gelu, na proužku modifikované celulosy apod.) gradient pH; poté se nanese vzorek (směs bílkovin nebo peptidů) a vloží se stejnosměrné elektrické pole. Jednotlivé molekuly dělených amfiontů se pohybují podle svého okamžitého náboje až do místa, kde pH okolí odpovídá jejich isoelektrickému bodu (proto isoelektrická); zde se zastaví a zaostří (proto fokusace). Díky zaostření vykazuje tato metoda mimořádnou rozlišovací schopnost; lze oddělit bílkoviny lišící se v hodnotách isoelektrických bodů o pouhých 0,01. IEF bývá často kombinována s dalšími elektromigračními technikami (viz dvojrozměrná elektroforéza). | |
fosfát anorganickýangl. inorganic phosphate, anion kyseliny trihydrogenfosforečné (H3PO4), v biochemii běžně užívaná zkratka Pi. | |
fosfatasyangl. phosphatases, skupina enzymů ze třídy
hydrolas (EC 3.1.3.-), které odštěpují esterově vázaný zbytek kyseliny fosforečné. Například v glukogenesi se uplatňují při odštěpování fosfátového zbytku z fruktosa-1,6-bisfosfátu (fruktosa-1,6-bisfosfatasa, EC 3.1.3.11) a z glukosa-6-fosfátu (glukosa-6-fosfatasa, EC 3.1.3.9). Proteinfosfátfosfatasy hrají významnou roli při regulaci enzymové aktivity. V klinické biochemii se v krevním séru stanovují dva isoenzymy: aktivita alkalické fosfatasy (optimum pH nad 7, obvykle 8 až 9, EC 3.1.3.1) bývá zvýšena při onemocněních kostí, zatímco aktivita kyselé fosfatasy (optimum pH pod 7, obvykle 5 až 6, EC 3.1.3.2) při karcinomu prostaty. | |
fosfatidátyangl. phosphatidates, soli (anionty) fosfatidové kyseliny. | |
fosfatidytéž (ne zcela šťastně) glycerofosfolipidy nebo fosfoglyceridy, angl. phosphatides, estery kyseliny fosfatidové. Nejvýznamnějšími | |
fosfatidylinositolytéž fosfoinositidy, angl. phosphatidylinositols, estery fosfatidové kyseliny a cyklického alkoholu inositolu, který je 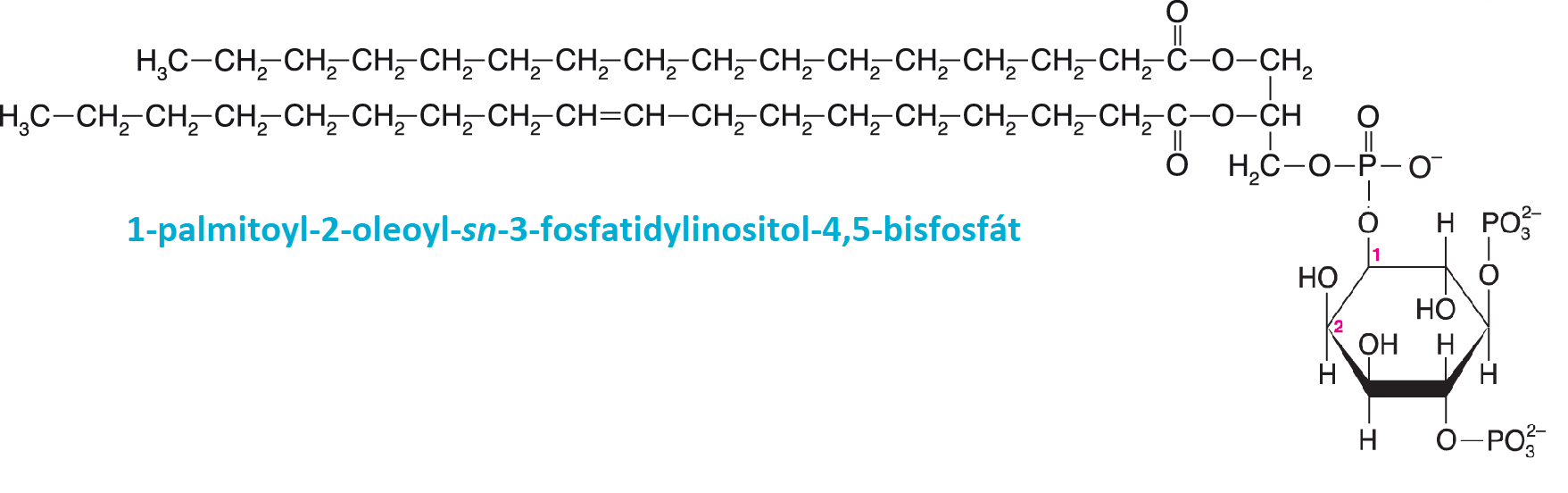 obvykle dále fosforylován. Z pravděpodobně nejvýznamnějšího fosforylovaného fosfatidylinositolu, fosfatidylinositolu-4,5-bisfosfátu (PIP2), se hydrolytickým štěpením fosfolipasou C uvolňuje inositol-1,4,5-trisfosfát (IP3) a diacylglycerol, které působí v buňkách jako druzí poslové. | |
fosfoadenosinfosfosulfátpřesněji 3´-fosfoadenosin-5´-fosfosulfát, angl. phosphoadenosine 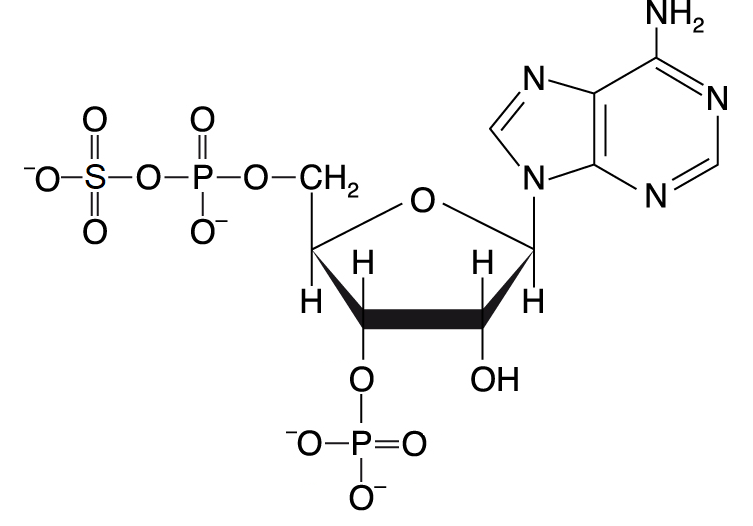 phosphosulphate, zkratka PAPS, aktivní sulfát, koenzym transferas přenášejících sulfátovou skupinu. Je zdrojem sulfátové skupiny při biosyntéze esterů kyseliny sírové (např. deriváty sacharidů, některé cerebrosidy). phosphosulphate, zkratka PAPS, aktivní sulfát, koenzym transferas přenášejících sulfátovou skupinu. Je zdrojem sulfátové skupiny při biosyntéze esterů kyseliny sírové (např. deriváty sacharidů, některé cerebrosidy). | |
fosfodiesterasyangl. phosphodiesterases, enzymy hydrolyzující
fosfodiesterové vazby (EC 3.1.4.-). Specifické fosfodiesterasy štěpí cyklické nukleosidmonofosfáty (cAMP a cGMP) na nukleosidmonofosfáty (5´-AMP a 5´-GMP, EC 3.1.4.53, EC 3.1.4.17) a podílejí se tak na regulaci hladiny těchto druhých poslů v buňkách. Do skupiny fosfodiesteras, podílejících se na buněčné signalizaci (viz dráhy signální), patří i fosfolipasy C (EC 3.1.4.11) a D (EC 3.1.4.50). Ačkoli jsou (deoxy)ribonukleotidy v nukleových kyselinách spojeny fosfodiesterovými vazbami, enzymový katalog ribonukleasy ani deoxyribonukleasy (endonukleasy a exonukleasy) mezi fosfodiesterasy neřadí. | |
fosfoenolpyruvátpřesněji 2-fosfoenolpyruvát, zkr. PEP, angl. phosphoenolpyruvate, důležitá makroergická sloučenina, 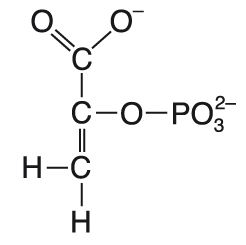 meziprodukt glykolysy a glukogenese, akceptor CO2 v cyklu C4-rostlin. Svůj fosfátový zbytek může předat ADP za vzniku ATP a pyruvátu (substrátová fosforylace). meziprodukt glykolysy a glukogenese, akceptor CO2 v cyklu C4-rostlin. Svůj fosfátový zbytek může předat ADP za vzniku ATP a pyruvátu (substrátová fosforylace). | |
fosfofruktokinasaangl. phosphofructokinase, EC 2.7.1.11, enzym zodpovědný za regulaci glykolysy u savců. Katalyzuje fosforylaci fruktosa-6-fosfátu: fruktosa-6-fosfát + ATP → fruktosa-1,6- bisfosfát + ADP. Jaterní enzym je allostericky inhibován meziprodukty glykolysy a citrátového cyklu (fosfoenolpyruvátem a citrátem) a především ATP (indikátor "energetického dostatku"); jejich vazbou je enzym stabilizován v neaktivním stavu a tím je snížena jeho afinita k fruktosa-6-fosfátu. ADP a AMP (indikátory "energetické nouze") naopak stabilizují enzym v aktivním stavu a zvyšují tak afinitu k substrátům (fruktosa-6-fosfát a ATP). Tento enzym je také regulován hormonálně prostřednictvím insulinu. | |
fosfolipasyangl. phospholipases, skupina hydrolas, které štěpí fosfolipidy, zejména fosfatidy. Podle místa štěpení fosfatidů je 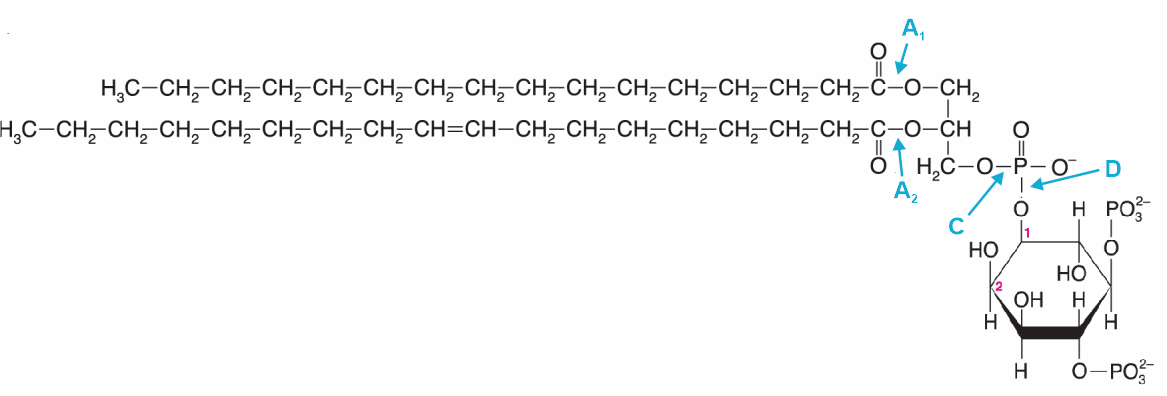 dělíme na fosfolipasu A1 (EC 3.1.1.32) odštěpující mastné kyseliny v poloze 1 glycerolu (např. palmitovou kyselinu z fosfolipidu na obr.), fosfolipasu A2 (EC 3.1.1.4, odštěpující olejovou kyselinu v poloze 2 ), fosfolipasu C (EC 3.1.4.3) štěpící vazbu mezi fosfátem a diacylglycerolem (na obr., vzniká IP3), a fosfolipasu D (EC 3.1.4.4), odštěpující alkohol z fosfatidové kyseliny (na obr., vzniká inositol-4,5-bisfosfát). Běžně se užívají zkratky PLA1, PLA2, PLC a PLD. Fosfolipasy se podílejí na odbourávání fosfolipidů, některé z nich, zejména PLC a PLD, hrají významnou roli při přenosu signálu (viz fosfatidylinositoly). dělíme na fosfolipasu A1 (EC 3.1.1.32) odštěpující mastné kyseliny v poloze 1 glycerolu (např. palmitovou kyselinu z fosfolipidu na obr.), fosfolipasu A2 (EC 3.1.1.4, odštěpující olejovou kyselinu v poloze 2 ), fosfolipasu C (EC 3.1.4.3) štěpící vazbu mezi fosfátem a diacylglycerolem (na obr., vzniká IP3), a fosfolipasu D (EC 3.1.4.4), odštěpující alkohol z fosfatidové kyseliny (na obr., vzniká inositol-4,5-bisfosfát). Běžně se užívají zkratky PLA1, PLA2, PLC a PLD. Fosfolipasy se podílejí na odbourávání fosfolipidů, některé z nich, zejména PLC a PLD, hrají významnou roli při přenosu signálu (viz fosfatidylinositoly). | |
fosfolipidyangl. phospholipids, lipidy obsahující fosfátový zbytek; biologicky velmi významná skupina složených
lipidů, tvořících základní složku biologických membrán. Chemicky to jsou zejména:
| |
fosfoproteinyangl. phosphoproteins, složené bílkoviny, jejichž prostetickou skupinou je kyselina fosforečná (resp. anorganický fosfát), většinou vázaná na hydroxylové skupiny postranních řetězců serinu, threoninu nebo tyrosinu esterovou vazbou. Dočasná fosforylace enzymů patří k nejdůležitějším způsobům regulace jejich aktivity. Trvale fosforylované bílkoviny jsou obsaženy ve velkém množství v mléce (kasein) a ve vejcích (ovalbumin, fosfovitin); mezi trvalé fosfoproteiny patří i pepsin. | |
fosforylaceangl. phosphorylation, připojení zbytku kyseliny fosforečné, lépe řečeno enzymově katalyzovaná tvorba jejích esterů či anhydridů. Nejčastějším způsobem fosforylace je přenos zbytku kyseliny fosforečné z
ATP na substrát (např. ATP + glukosa → ADP + glukosa-6-fosfát); tuto reakci katalyzují fosfotransferasy zvané kinasy. Fosforylace se významně podílí na regulaci biologických dějů (viz enzymy – regulace aktivity, též proteinkinasy). Opačný děj (defosforylace), tj. odstranění fosfátové skupiny z organické molekuly, je zprostředkován skupinou enzymů zvaných fosfatasy. Velmi významné jsou fosforylace, jimiž se syntetizuje ATP z ADP (viz fosforylace membránová, fosforylace oxidační a fosforylace substrátová, též fotofosforylace). | |
fosforylace membránováangl. membrane phosphorylation, reakce, při níž je k molekule
ADP připojován (anorganický) fosfátový zbytek: ADP + Pi → ATP + H2O, přičemž tato endergonická reakce získává energii tím, že je spřažena s pasivním transportem protonů biologickou membránou; probíhá tedy na úkor proton-motivní síly. Proces je katalyzován ATP-synthasou. Proton-motivní síla nutná pro tento děj je generována oxidačně-redukčními reakcemi buď v dýchacím řetězci (viz fosforylace oxidační), nebo ve světlé fázi fotosyntézy (viz fotofosforylace). | |
fosforylace oxidačnítéž oxidativní, angl. oxidative phosphorylation, membránová fosforylace u organismů využívajících dýchací řetězec pro generování proton-motivní síly, jeden z nejdůležitějších procesů bioenergetiky. Konečným akceptorem elektronů v dýchacím řetězci může být molekulový kyslík (proto též fosforylace aerobní) nebo jiný extracelulární akceptor elektronů, např. dusičnanový nebo síranový ion (viz anaerobní respirace). Primárním "dodavatelem" elektronů do tohoto procesu jsou u organotrofních organismů organické látky (resp. redukované kofaktory), u chemolithotrofních organismů látky anorganické (sulfan, amoniak, Fe2+ apod.). | |
fosforylace substrátováangl. substrate-level phosphorylation, vedle
membránové fosforylace jediný způsob syntézy nukleosidtrifosfátů, zejména ATP. Jedná se buď o přenos fosfátového zbytku z makroergického substrátu (fosfoenolpyruvátu, 1,3-bisfosfoglycerátu, kreatinfosfátu) na ADP pomocí enzymů z třídy transferas, nebo o obrácenoureakci katalyzovanou ligasou (např. sukcinyl-CoA + GDP + Pi → sukcinát + CoA + GTP, sukcinyl-CoA-ligasa, EC 6.2.1.4, reakce citrátového cyklu). | |
fosforylasyangl. phosphorylases, skupina enzymů z třídy
transferas (EC 2.4.1.-), které katalyzují vznik fosforečných esterů sacharidů přenosem cukerného zbytku z oligosacharidu nebo polysacharidu na anorganický fosfát. Nejdůležitější reakcí tohoto typu je přenos zbytku glukosy z glykogenu na fosfátový ion za vzniku glukosa-1-fosfátu: (glukan)n + Pi → (glukan)n-1 + glukosa-1-fosfát (glykogenfosforylasa, EC 2.4.1.1) | |
fotofosforylaceangl. photophosphoralytion, syntéza
ATP při fotosyntéze, probíhající podle rovnice ADP + Pi → ATP + H2O. Jedná se o typ membránové fosforylace, kdy proton-motivní síla je generována na úkor zachycené světelné energie. Rozlišují se dva způsoby provedení tohoto děje:
| |
fotolýza vodytéž Hillova reakce, angl. water photolysis, rozklad vody při
fotosyntéze u sinic, řas a vyšších rostlin. Po absorpci světelného kvanta se z molekuly chlorofylu v reakčním centru fotosystému II uvolní elektron, který je použit v dalších reakcích fotosyntézy; tento elektron je posléze nahrazen elektronem z molekuly vody a molekulový kyslík se uvolňuje. Obvykle se tato reakce vyjadřuje v symbolické podobě: 2 H2O → O2 + 4 H+ + 4 e-. Vzhledem k tomu, že uvolněný elektron ve skutečnosti nahrazuje elektron, použitý pro redukci NADP, je lépe celkovou bilanci děje vyjádřit jako: H2O + NADP+→ ½ O2 + NADPH + H+ (viz fotoredukce). Atom kyslíku ve vodě zde působí, v rozporu se vší chemickou zkušeností (kyslík se přece považuje za prototyp oxidačního činidla), jako redukční činidlo. Fotolýza vody je jediným zdrojem molekulového kyslíku na Zemi. | |
fotoredukceangl. photoreduction, redukce
NADP+ při fotosyntéze: NADP+ + 2 e- + H+ → NADPH. V celkové bilanci fotosyntézy může být zdrojem elektronů voda (viz fotolýza vody) nebo jiný zdroj elektronů (viz oxygenní a anoxygenní fotosyntéza). | |
fotorespiraceangl. photorespiration, světelné dýchání rostlin. Enzym ribulosa-1,5-bisfosfátkarboxylasa/oxygenasa (viz RUBISCO) má schopnost 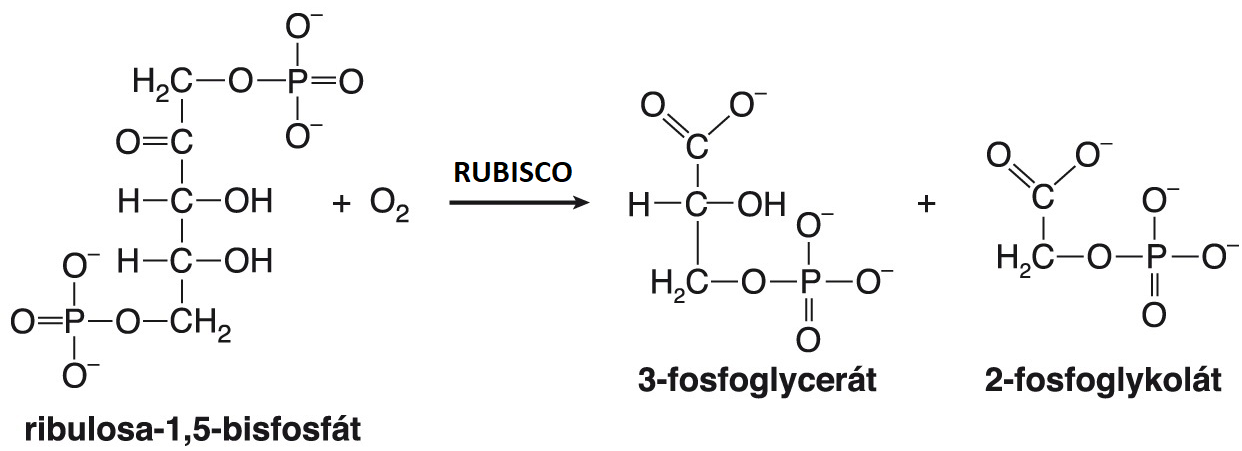 vázat na substrát (ribulosa-1,5-bisfosfát) oxid uhličitý, ale také kyslík. K fotorespiraci dochází oxygenasovou aktivitou tohoto enzymu. Po navázání kyslíku vzniká nestálý meziprodukt s pěti atomy uhlíku, který se rozpadá na dva produkty, jeden se třemi a druhý se dvěma atomy uhlíku. Tříuhlíkatý produkt (3-fosfoglycerát) vstupuje do reakcí Calvinova cyklu, dvouuhlíkatý (2-fosfoglykolát) je dále metabolizován v peroxisomu na glyoxylát, který může přijmout aminoskupinu a stát se tak prekursorem syntézy glycinu a následně serinu. Většina glyoxylátu je však katabolizována až na CO2, a proto fotorespirace působí značný pokles produkce sacharidů. Dochází k ní především u C3-rostlin (viz rostliny C3, C4 a CAM), kde může způsobit ztrátu 20 až 40 % primárně zachyceného CO2. | |
fotosyntézaangl. photosynthesis, proces zahrnující zachycení energie světelného záření, její uložení ve formě energie chemických vazeb a její následné využití pro přeměnu anorganických látek (zejména
CO2) na látky organické. Fotosyntéza je nejdůležitější biochemický proces na Zemi. Probíhá v zelených částech rostlin, fototrofních bakteriích a řasách. U eukaryot je lokalizována v chloroplastech, specializovaných organelách obsahujících chlorofyl. Ve vnitřních membránách chloroplastů (thylakoidech) jsou zakotveny dva typy fotosystémů absorbujících světelnou energii. Takto získaná energie je ve světlé fázi fotosyntézy přímo využita k redukci NADP+ na NADPH (viz fotoredukce), ale také uložena do formy proton-motivní síly a následně do chemické struktury ATP (viz fotofosforylace). Tyto látky jsou nezbytné pro následující temnou fázi fotosyntézy, kde se zabudovává CO2 (v Calvinově cyklu), ale také anorganický dusík a síra do organických sloučenin. Podle prvních kroků fixace CO2 dělíme rostliny na C3, C4 a CAM (viz rostliny C3, C4 a CAM). | |
fotosyntéza oxygenní a anoxygenníangl. oxygenic and anoxygenic fotosynthesis, dvě varianty světlé fáze fotosyntézy. Při oxygenní fotosyntéze je donorem elektronů pro fotoredukci voda (resp. její kyslík, viz fotolýza vody), při anoxygenní nějaký jiný donor elektronů. Anoxygenní fotosyntéza je vývojově starší forma, v současnosti přetrvávající pouze u některých bakterií, které mohou být fotolithotrofní nebo fotoorganotrofní (viz organismy – rozdělení podle způsobu výživy). Donorem vodíku pro fotoredukci je u fotolithotrofních bakterií nejčastěji sulfan (produkují síru), u fotoorganotrofních bakterií organická látka, např. 2-propanol (produkují aceton) nebo mastná kyselina. Konečným akceptorem vodíku je vždy oxid uhličitý, který je, jako při každém fotosyntetickém procesu, redukován a zabudován do organických molekul, především do sacharidů. Protože při anoxygenní fotosyntéze mají donory elektronů nižší redoxní potenciál (jsou slabšími oxidačními činidly) než kyslík a uvolňují tedy elektron snáze, mohou fotosyntetizující bakterie vystačit s jediným fotosystémem. | |
fotosystémyangl. photosystems, membránové strukturní jednotky zachycující a využívající světelnou energii, též
kvantosomy. Jsou uloženy ve velkém množství ve vnitřních membránách chloroplastů (v thylakoidech). Rozlišujeme dva typy, fotosystém I a fotosystém II (PS I a PS II). Jsou tvořeny anténním komplexem (LHC) a reakčním centrem (RC). Molekuly LHC absorbují světelnou energii a přenášejí ji do RC, kde je přítomen chlorofyl a, vázaný na specifický protein. Při excitaci se dramaticky sníží redoxní potenciál tohoto chlorofylu, který se tak stává silným redukčním činidlem a je schopen přenést svůj elektron na molekulu příslušného přenašeče. Absorpční maximum chlorofylu a v PS I je 700 nm, v PS II 680 nm, proto jsou někdy označovány jako fotosystém P700 a P680. | |
fragmenty Okazakihoangl. Okazaki fragments, polydeoxyribonukleotidy, které jsou syntetizovány při
replikaci jakožto úseky zpožďujícího se řetězce, aby byly posléze spojeny DNA-ligasou a vytvořily jediné vlákno. Každý úsek se syntetizuje jako samostatná jednotka včetně iniciace pomocí RNA-polymerasy. U prokaryot mají Okazakiho fragmenty délku 1 000 až 2 000 deoxyribonukleotidů, u eukaryot jsou mnohem kratší (100 až 200 deoxyribonukleotidů). | |
fruktosatéž ovocný cukr, angl. fructose, nejrozšířenější ketohexosa, nejsladší 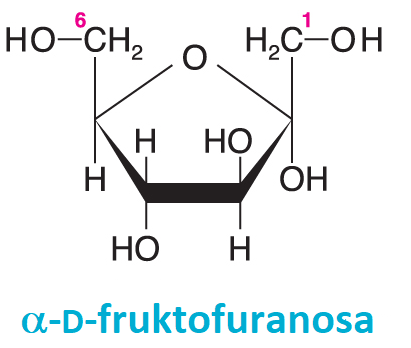 přírodní cukr. Jako všechny významné monosacharidy existuje v přírodě téměř výhradně v konfiguraci D; otáčí však rovinu lineárně polarizovaného světla vlevo, proto se pro ni používá tradiční synonymum levulosa. Fruktosa se vyskytuje v různých rostlinných šťávách a v medu. Je rychleji stravitelná než glukosa. Disacharid tvořený fruktosou a glukosou je sacharosa. Fruktosa (resp. její aktivované formy, fruktosa-6-fosfát a fruktosa-1,6-bisfosfát) jsou meziprodukty glykolysy, glukogenese, pentosového a Calvinova cyklu. Fruktosa-2,6-bisfosfát je důležitým regulačním metabolitem. přírodní cukr. Jako všechny významné monosacharidy existuje v přírodě téměř výhradně v konfiguraci D; otáčí však rovinu lineárně polarizovaného světla vlevo, proto se pro ni používá tradiční synonymum levulosa. Fruktosa se vyskytuje v různých rostlinných šťávách a v medu. Je rychleji stravitelná než glukosa. Disacharid tvořený fruktosou a glukosou je sacharosa. Fruktosa (resp. její aktivované formy, fruktosa-6-fosfát a fruktosa-1,6-bisfosfát) jsou meziprodukty glykolysy, glukogenese, pentosového a Calvinova cyklu. Fruktosa-2,6-bisfosfát je důležitým regulačním metabolitem. | |
furanosyangl. furanoses, cyklické formy monosacharidů, formálně | |
Furchgott Robert Francis
| |
fúze buněčnáangl. cell fusion, přirozené nebo uměle vyvolané spojení obsahu dvou
buněk bez toho, že by obsah jedné z nich byl následně zničen (srov. fagocytóza). Fúzí vzniká hybridní buňka, nesoucí znaky obou původních buněk. Přirozeně k ní dochází při splynutí pohlavních buněk, při kopulaci kvasinek a při spojování svalových buněk. Uměle může být vyvolána polyethylenglykolem (viz hybridomové technologie), elektrickým výbojem apod. | |
fylogenezeangl. phylogenesis, vývoj
biologických druhů, základní proces z pohledu evoluční teorie (srov. ontogeneze = vývoj jedince). | |




 německý chemik (1852–1919), Nobelova cena (chemie, 1902) za syntézy
německý chemik (1852–1919), Nobelova cena (chemie, 1902) za syntézy 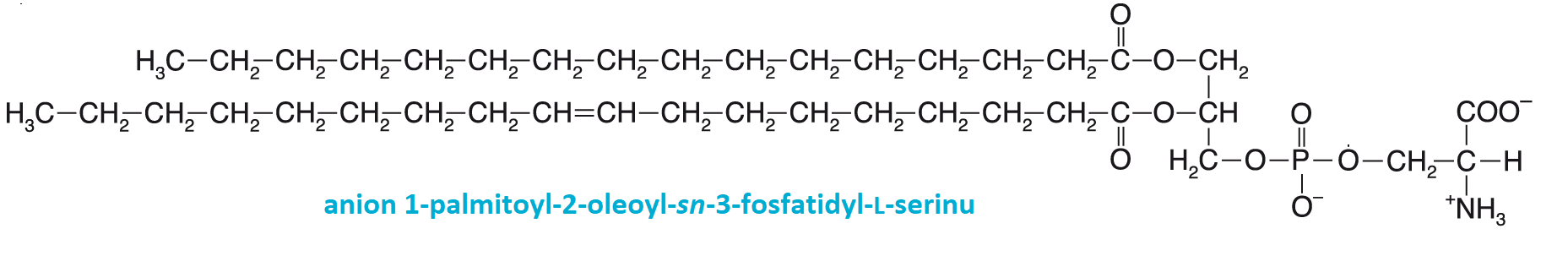 strukturními fosfatidy, které tvoří základ
strukturními fosfatidy, které tvoří základ 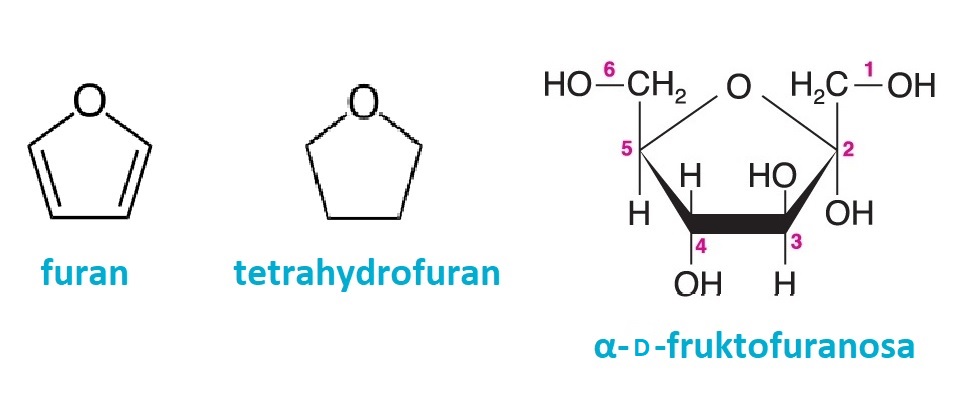 odvozené od pětičlenného heterocyklu furanu.
odvozené od pětičlenného heterocyklu furanu.  americký biochemik a farmakolog (1916–2009), Nobelova cena (za fyziologii a lékařství, 1998) za objevy vysvětlující působení
americký biochemik a farmakolog (1916–2009), Nobelova cena (za fyziologii a lékařství, 1998) za objevy vysvětlující působení