Biochemický slovník
Biochemický slovník
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
S |
|---|
S-adenosylmethioninaktivní methyl, angl. S-adenosyl-methionine, zkr. SAM nebo AdoMet, 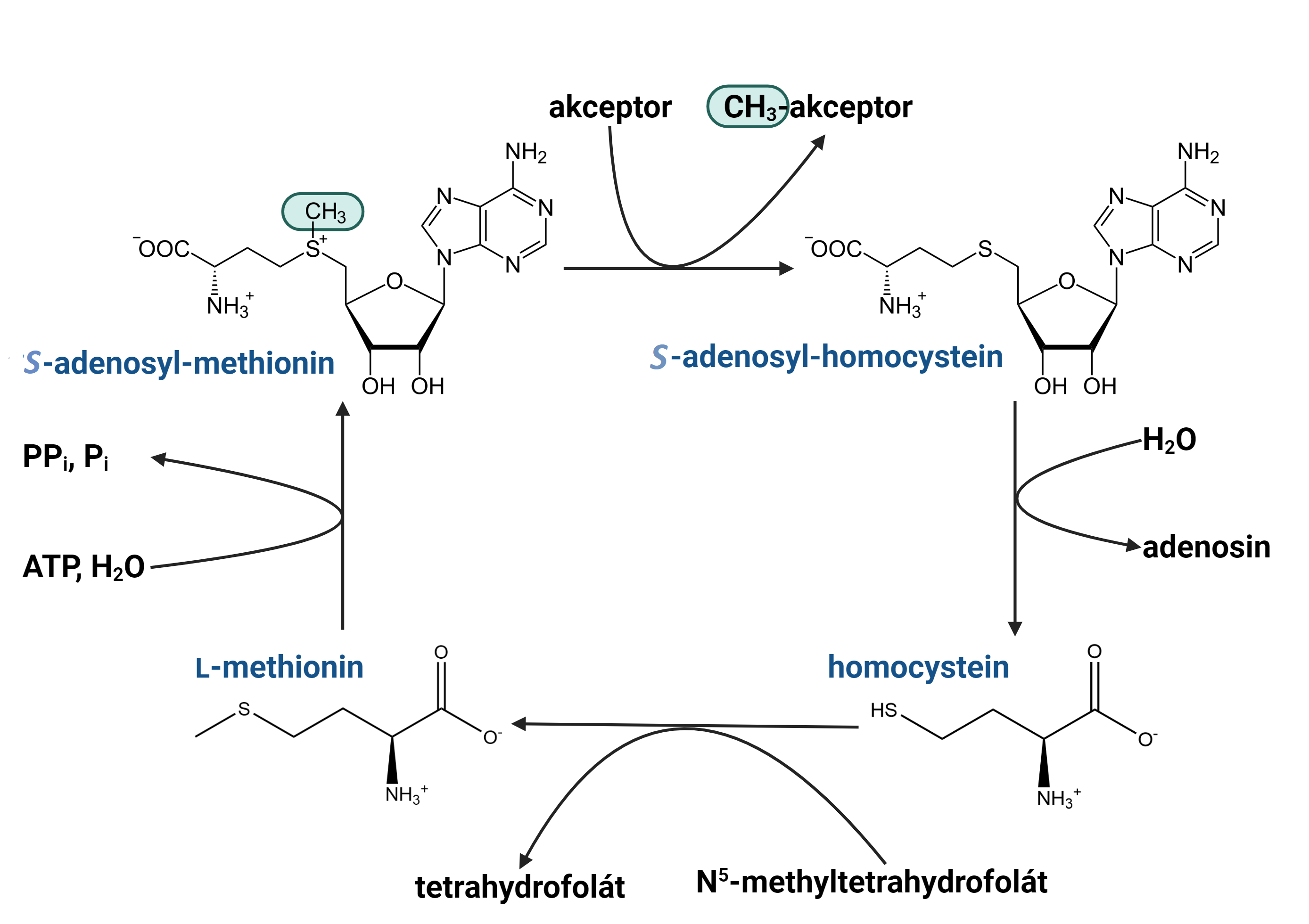 methylační činidlo buněk, koenzym transferas. Methylace tímto koenzymem se využívá např. při vzniku fosfatidylcholinu z fosfatidylethanolaminu (viz fosfatidy), při methylačních modifikacích DNA, tRNA a rRNA nebo při methylacích souvisejících se vznikem čepičky mRNA. Vzniká přenosem adenosylu z ATP na atom síry methioninu, čímž se aktivuje methylová skupina. Po jejím předání akceptoru se hydrolyticky odštěpuje adenosylový zbytek a vzniklý homocystein může být převeden na methionin; methylačním činidlem této reakce je N5-methyltetrahydrofolát.
Souhrnně lze tedy tento cyklus popsat rovnicí: N5-methyltetrahydrofolát + akceptor + ATP + 2 H2O → tetrahydrofolát + akceptor-CH3 + adenosin + PPi + Pi. methylační činidlo buněk, koenzym transferas. Methylace tímto koenzymem se využívá např. při vzniku fosfatidylcholinu z fosfatidylethanolaminu (viz fosfatidy), při methylačních modifikacích DNA, tRNA a rRNA nebo při methylacích souvisejících se vznikem čepičky mRNA. Vzniká přenosem adenosylu z ATP na atom síry methioninu, čímž se aktivuje methylová skupina. Po jejím předání akceptoru se hydrolyticky odštěpuje adenosylový zbytek a vzniklý homocystein může být převeden na methionin; methylačním činidlem této reakce je N5-methyltetrahydrofolát.
Souhrnně lze tedy tento cyklus popsat rovnicí: N5-methyltetrahydrofolát + akceptor + ATP + 2 H2O → tetrahydrofolát + akceptor-CH3 + adenosin + PPi + Pi. | |
sacharidyangl. saccharides, monosacharidy a jejich kondenzační produkty – oligosacharidy a polysacharidy. Jsou přítomny ve všech organismech, kde plní několik významných funkcí:
| |
sacharidy redukující
| |
sacharosaangl. sucrose, třtinový nebo řepný cukr, α-D-glukopyranosyl-β-D-fruktofuranosid, 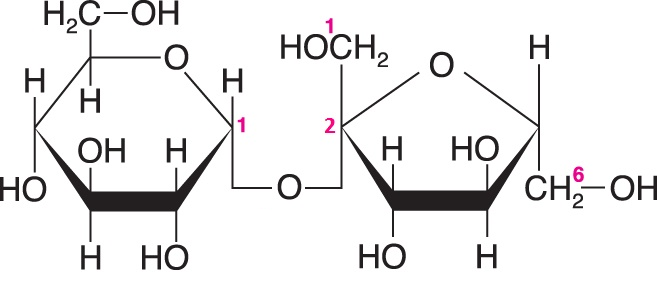 neredukující disacharid. Vzniká přenosem glukosylového zbytku z UDP-glukosy na fruktosu. Je důležitým metabolickým produktem všech zelených rostlin, kde slouží jako transportní rozpustný sacharid; živočichové ji nesyntetizují. V kyselém prostředí hydrolyzuje na ekvimolární směs glukosy a fruktosy (viz invertní cukr); stejnou reakci za neutrálních podmínek katalyzuje enzym sacharasa (též invertasa). Sacharosa se používá jako sladidlo v potravinářství. Může být zkvašována mikroorganismy, ale ve vyšších koncentracích inhibuje jejich růst – proto se používá jako konzervační činidlo (marmelády apod.). neredukující disacharid. Vzniká přenosem glukosylového zbytku z UDP-glukosy na fruktosu. Je důležitým metabolickým produktem všech zelených rostlin, kde slouží jako transportní rozpustný sacharid; živočichové ji nesyntetizují. V kyselém prostředí hydrolyzuje na ekvimolární směs glukosy a fruktosy (viz invertní cukr); stejnou reakci za neutrálních podmínek katalyzuje enzym sacharasa (též invertasa). Sacharosa se používá jako sladidlo v potravinářství. Může být zkvašována mikroorganismy, ale ve vyšších koncentracích inhibuje jejich růst – proto se používá jako konzervační činidlo (marmelády apod.). | |
Sakmann Bert
| |
Samuelsson Bengt Ingemar
| |
Sancar Aziz
| |
Sanger Frederick anglický biochemik (1918–2013), získal dvě Nobelovy ceny za chemii: za práci na struktuře proteinů, zvláště insulinu (1958) a spolu s W. Gilbertem za příspěvek ke stanovení sekvence bází v nukleových kyselinách (1980). Studoval v Cambridge biologii; dle svého vyjádření byl průměrným studentem. Během studia ho zaujala biochemie, z níž pak získal doktorát. Od roku 1943 se věnoval výzkumu proteinů a zvláště insulinu. V této době již byly známy účinné metody izolace proteinů a byla tedy reálná možnost stanovit jejich strukturu. Sanger vypracoval metodu sekvenování proteinů; během zhruba desetiletého úsilí vyřešil kompletní primární strukturu insulinu. Kolem roku 1960 se začal zajímat o nukleové kyseliny a v roce 1962, již jako nositel Nobelovy ceny, přešel do nově vybudovaných laboratoří molekulární biologie v Cambridge, kde spolupracoval s M. F. Perutzem, F. H. C. Crickem, J. C. Kendrewem a A. Klugem. Zde nejprve vypracoval metody stanovení krátkých sekvencí RNA. Jeho práce kulminovala kolem roku 1975 vypracováním enzymové dideoxy-techniky sekvenování DNA. V současné době je metoda automatizovaná a používá se ve zmodernizované formě např. k sekvenaci genomu různých organismů. | |
sedimentaceusazování, angl. sedimentation, v laboratorní a klinické biochemii zejména
| |
sekvenceangl. sequence, pořadí monomerních jednotek v (bio)polymeru nebo jeho části (viz primární struktura), pojem se používá též pro úsek polymerního řetězce jisté struktury (např. vedoucí sekvence v bílkovině a v mRNA, pre-sekvence a pro-sekvence v bílkovinách). | |

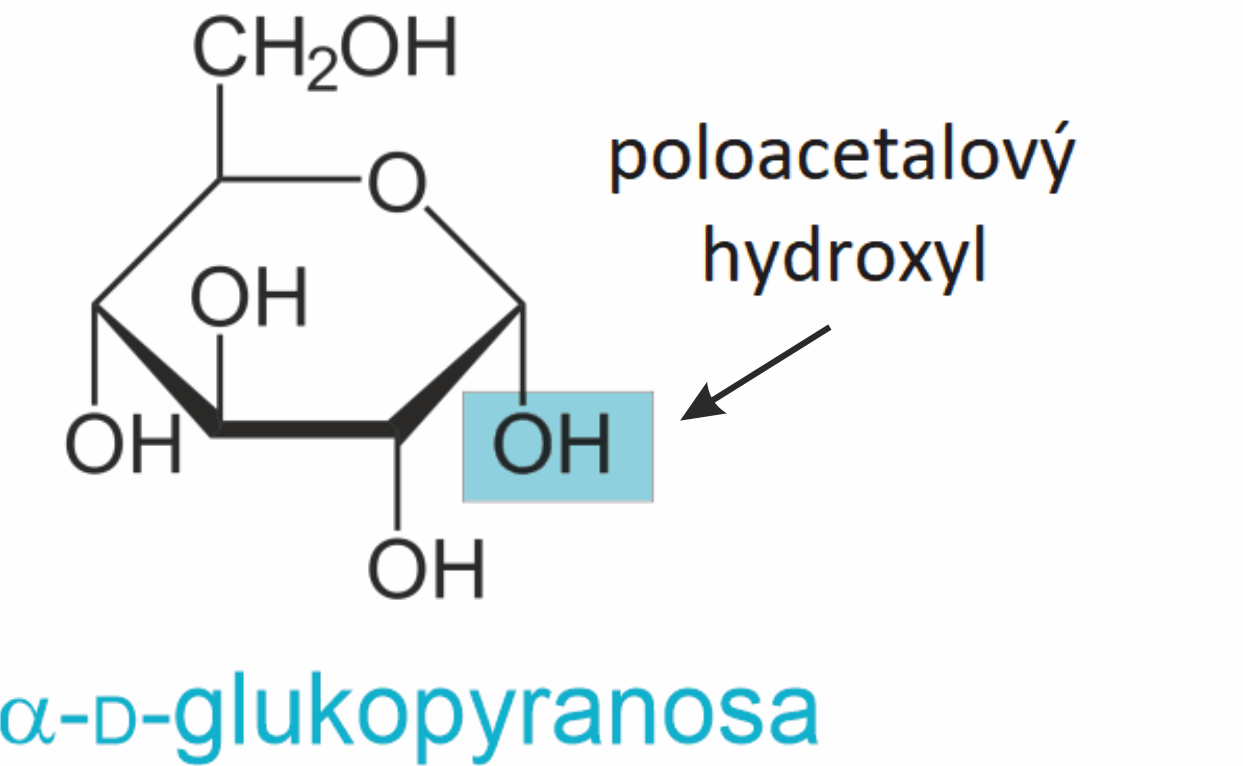 angl. reducing
angl. reducing 

 turecký lékař a biochemik (nar. 1946), Nobelova cena (chemie, 2015) za výzkum
turecký lékař a biochemik (nar. 1946), Nobelova cena (chemie, 2015) za výzkum