Biochemický slovník
Biochemický slovník
Procházet slovníkem pomocí tohoto rejstříku
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
K |
|---|
koenzymyangl. coenzymes, skupina nízkomolekulárních látek (viz kofaktory enzymů), podílejících se na enzymové reakci tím, že přenášejí chemické skupiny, elektrony nebo atomy vodíku. Koenzym tedy propojuje dvě nezávislé reakce katalyzované odlišnými enzymy a může být považován za transportní metabolit; v intracelulárním prostředí se vyskytuje volný ve dvou (nejméně) formách. Koenzymy jsou substráty reakcí a jako takové jsou uváděny v enzymovém katalogu; někdy se hovoří o kosubstrátech. Typickým koenzymem je NAD+, který může přijmout vodíky např. od ethanolu, CH3-CH2OH + NAD+ → CH3-CHO + NADH + H+ (enzym alkoholdehydrogenasa, EC 1.1.1.1); regeneruje (oxiduje) se pak většinou v dýchacím řetězci, kde vodíky předá koenzymu Q: NADH + H+ + Q → NAD+ + QH2 (enzym ubichinonreduktasa, též kotvený komplex I, EC 7.1.1.2). Termínu koenzym se v některých učebnicích (nepříliš šťastně) používá též pro prostetické skupiny enzymů. | |
kofaktory enzymůangl. enzyme cofactors, nízkomolekulární struktury uplatňující se při enzymových reakcích; bez jejich přítomnosti by reakce neprobíhala. Do této skupiny látek patří:
| |
Köhler Georges Jean Franz
| |
kolagenangl. collagen, ve vodě nerozpustný extracelulární
skleroprotein (fibrilární protein). Obsahuje velké množství glycinu, prolinu a neproteinogenní aminokyseliny hydroxyprolin a hydroxylysin, které vznikají posttranslační modifikací (enzymovou hydroxylací za účasti askorbové kyseliny). Základní sekundární struktura je levotočivý helix, terciární struktura je tvořena třemi těmito helixy stočenými do velmi pevné pravotočivé šroubovice. Je základním stavebním materiálem pojivových a vazivových tkání, hlavní organickou složkou kůže, chrupavek, kostí, oční rohovky, cévních stěn, šlach a zubů. Tvoří 25 až 30 hmotn. % všech bílkovin v těle savců. Částečnou hydrolýzou se mění v rozpustnou želatinu, snadno tvořící gely. Používá se k výrobě želatiny, klihu, jako materiál pro chirurgická vlákna a obaly uzenin ( střívka). | |
koloběh dusíkuangl. nitrogen cycle, vzájemné přeměny sloučenin dusíku v biosféře. Jde 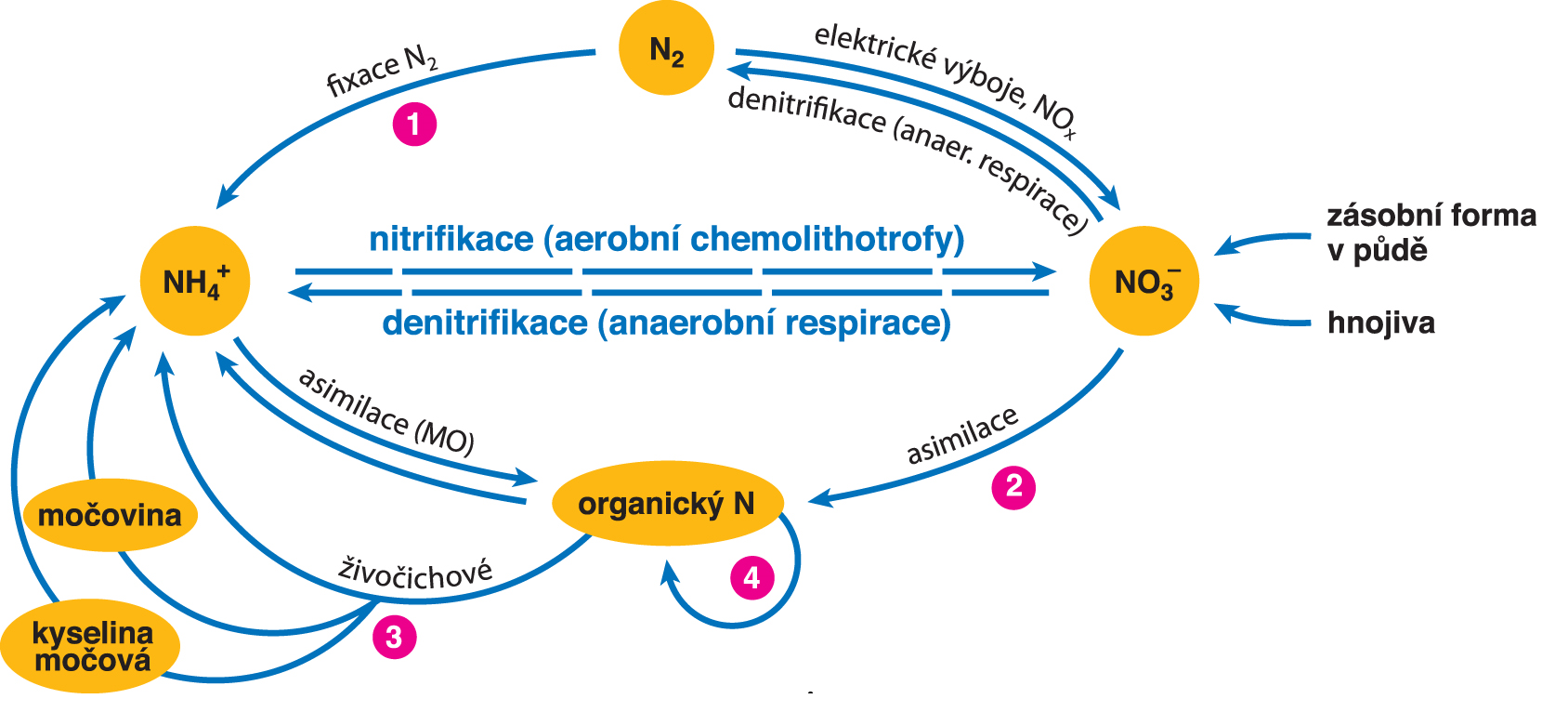 o komplexní proces, jehož se účastní dusík v mnoha podobách. Je zabudováván do organických sloučenin (především v oxidačním stavu
NIII-), ve vyšších oxidačních stavech (NV+ a NIII+)
slouží jako oxidační činidlo při anaerobní respiraci (denitrifikaci),
jeho největší zásoba je v atmosféře, kde je ve formě molekulárního
dusíku. o komplexní proces, jehož se účastní dusík v mnoha podobách. Je zabudováván do organických sloučenin (především v oxidačním stavu
NIII-), ve vyšších oxidačních stavech (NV+ a NIII+)
slouží jako oxidační činidlo při anaerobní respiraci (denitrifikaci),
jeho největší zásoba je v atmosféře, kde je ve formě molekulárního
dusíku. Poznámky k obr.: 1: viz bakterie hlízkové; 2: viz
nitrátreduktasa; 3: viz živočichové – rozdělení podle způsobu vylučování
dusíku; 4: viz transaminace, biosyntéza purinových a pyrimidinových
nukleotidů atd.; MO = mikroorganismy. | |
koloběh kyslíkuangl. oxygen cycle, soubor procesů, jimiž je do zemské atmosféry dodáván kyslík (viz oxygenní fotosyntéza, Hillova reakce) a naopak je aerobními organismy 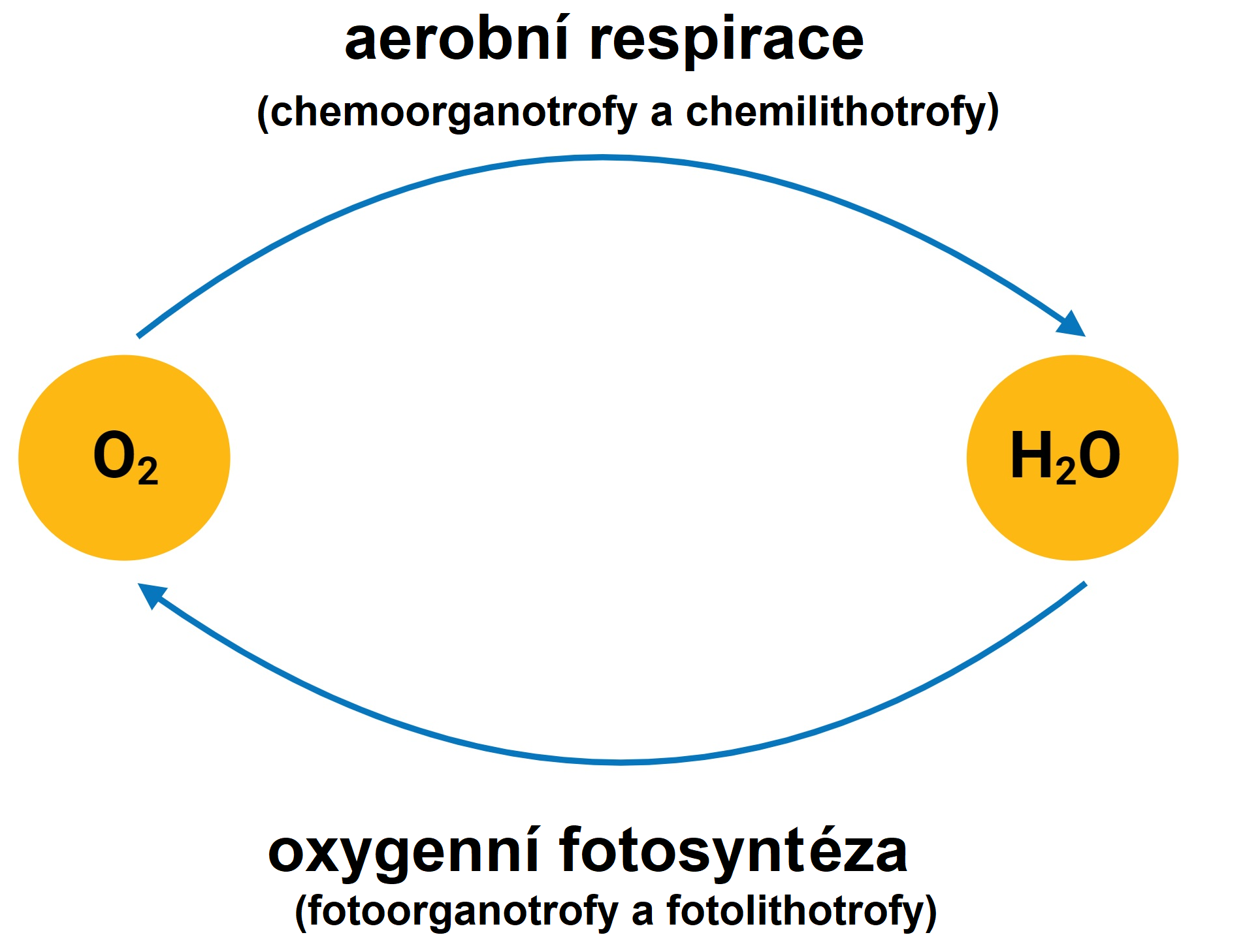 spotřebováván. Kyslík
slouží aerobům jako oxidační činidlo (viz aerobní respirace). Mohou jím
oxidovat organické (organotrofy) i anorganické (lithotrofy) látky,
v obou případech vzniká voda. Kyslík je také spotřebováván reakcemi,
katalyzovanými různými oxidasami a oxygenasami. spotřebováván. Kyslík
slouží aerobům jako oxidační činidlo (viz aerobní respirace). Mohou jím
oxidovat organické (organotrofy) i anorganické (lithotrofy) látky,
v obou případech vzniká voda. Kyslík je také spotřebováván reakcemi,
katalyzovanými různými oxidasami a oxygenasami. | |
koloběh síryangl. sulphur cycle, vzájemné přeměny sirných sloučenin v biosféře. Autotrofní organismy 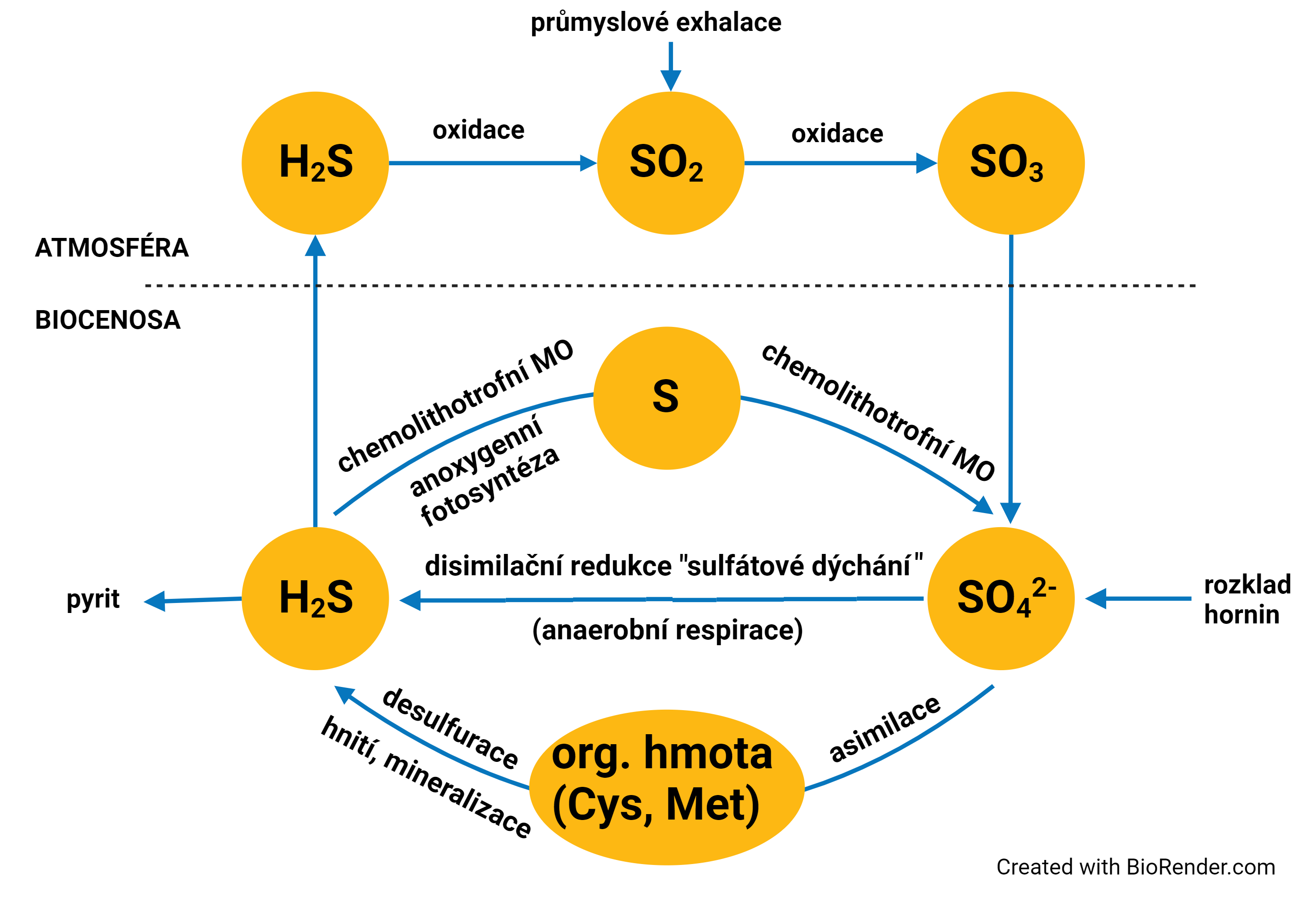 mohou přijímat síru v podobě jejích anorganických iontů (sulfidových,
siřičitanových, síranových nebo thiosíranových) či ve formě elementární
síry a zabudovávat ji do organických sloučenin. V procesu desulfurace se
při mineralizaci (hnití) organických sloučenin síra uvolňuje ve formě
sulfanu (H2S).
Pro některé fotosyntetizující bakterie slouží sulfan jako zdroj
vodíkových atomů (viz anoxygenní fotosyntéza). Autotrofní sirné bakterie
(chemolithotrofní mikroorganismy) využívají oxidaci redukovaných sirných
sloučenin (sulfanu, siřičitanu) jako zdroje energie. Některé respirující
anaerobní bakterie používají naopak síranové ionty jako oxidační činidlo
(viz anaerobní respirace). Heterotrofní organismy musí organicky
vázanou síru přijímat v potravě; sirné aminokyseliny (methionin a
cystein) mohou sice být metabolicky převáděny jedna na druhou, ale
alespoň jedna z nich je pro heterotrofy vždy esenciální. mohou přijímat síru v podobě jejích anorganických iontů (sulfidových,
siřičitanových, síranových nebo thiosíranových) či ve formě elementární
síry a zabudovávat ji do organických sloučenin. V procesu desulfurace se
při mineralizaci (hnití) organických sloučenin síra uvolňuje ve formě
sulfanu (H2S).
Pro některé fotosyntetizující bakterie slouží sulfan jako zdroj
vodíkových atomů (viz anoxygenní fotosyntéza). Autotrofní sirné bakterie
(chemolithotrofní mikroorganismy) využívají oxidaci redukovaných sirných
sloučenin (sulfanu, siřičitanu) jako zdroje energie. Některé respirující
anaerobní bakterie používají naopak síranové ionty jako oxidační činidlo
(viz anaerobní respirace). Heterotrofní organismy musí organicky
vázanou síru přijímat v potravě; sirné aminokyseliny (methionin a
cystein) mohou sice být metabolicky převáděny jedna na druhou, ale
alespoň jedna z nich je pro heterotrofy vždy esenciální. | |
kompartmentyangl. compartments, v biologii části systému oddělené od ostatních definovaným rozhraním. Z hlediska celého organismu považujeme za jeden kompartment např. krevní řečiště, obsah žaludku či dvanáctníku, mozkomíšní mok, oční sklivec apod. Buněčné kompartmenty
eukaryotních buněk jsou části buňky (viz organely) oddělené od ostatního prostoru (cytosolu) biologickou membránou, která zajišťuje selektivní komunikaci kompartmentu s okolím. Patří sem např. mitochondrie, chloroplasty, thylakoidy, lysosomy, peroxisomy, vakuoly a endoplasmatické retikulum, za samostatný kompartment je samozřejmě považován i cytosol. Buněčné kompartmenty obvykle obsahují různou enzymovou výbavu, což umožňuje paralelní průběh různorodých metabolických dějů a jejich regulaci. Tak např. glukosa je v cytosolu účinně aktivována převedením na glukosa-6-fosfát (katalýza enzymem hexokinasou, EC 2.7.1.1), opačná reakce, totiž hydrolýza glukosa-6-fosfátu na glukosu (glukosa-6-fosfátfosfatasa, EC 3.1.3.9) probíhá v endoplasmatickém retikulu. | |
komplementangl. complement, soubor asi 40 sérových (krevních) a membránových glykoproteinů, podílejících se u obratlovců na některých imunitních a alergických reakcích (např. ničení bakterií, likvidaci komplexů protilátky s antigenem, uvolňování histaminu). Jedná se o kaskádovitý systém, v němž každá aktivovaná složka je schopna vysoce specifickou proteolýzou aktivovat složku následující (srov. kaskáda koagulační). | |
komplementarita bazítéž párování bazí, angl. base complementarity / base pairing, schopnost bazí nukleových kyselin vytvářet pomocí vodíkových můstků 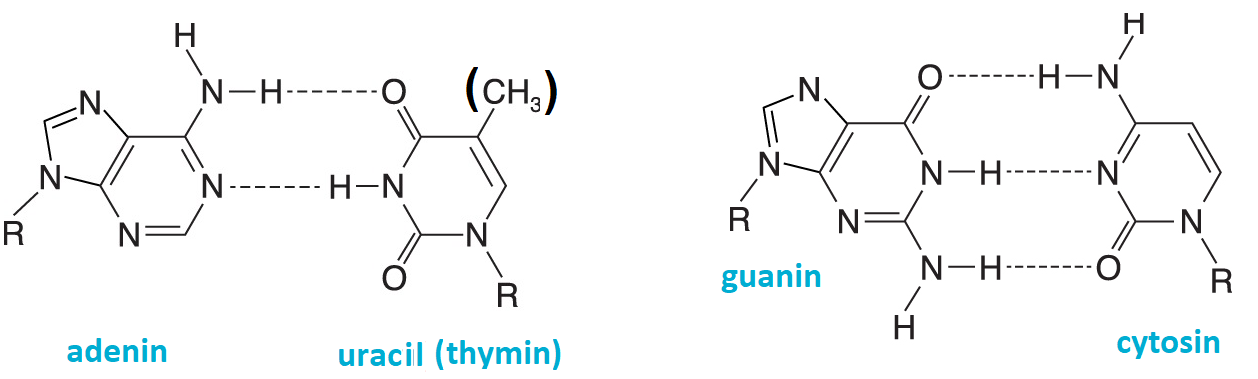 komplementární dvojice (A-T, A-U a G-C). Tato vlastnost je základem jejich funkce při uchovávání, předávání a
realizaci genetické informace v procesech replikace, transkripce a
translace. Komplementarita bazí je využívána i pro stabilizaci
prostorové struktury nukleových kyselin (dihelixů DNA, rRNA a tRNA). komplementární dvojice (A-T, A-U a G-C). Tato vlastnost je základem jejich funkce při uchovávání, předávání a
realizaci genetické informace v procesech replikace, transkripce a
translace. Komplementarita bazí je využívána i pro stabilizaci
prostorové struktury nukleových kyselin (dihelixů DNA, rRNA a tRNA). | |

