Biochemický slovník
Biochemický slovník
Procházet slovníkem pomocí tohoto rejstříku
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
R |
|---|
rovnice Hillovaangl. Hill equation, vztah mezi počáteční rychlostí enzymové reakce v0 u allosterických enzymů a koncentrací substrátu [S]: \( v_{0} = \frac{ V_{lim} . [S] ^{n} }{ K^{ `} + [S]^{n} } \) kde vlim je limitní rychlost (viz rovnice Michaelise a Mentenové), a K′ je konstanta, jen formálně připomínající Michaelisovu konstantu. Parametr n (často též označovaný α) se nazývá koeficient sigmoidity nebo též Hillův; čím vyšší má hodnotu, tím více se závislost v0 na [S] liší od hyperboly a má výraznější tvar sigmoidy. Hodnota n bývá často rovna počtu enzymově aktivních podjednotek v oligomerním enzymu, její hodnota roste při allosterické inhibici a klesá při allosterické aktivaci. Formálně podobným vztahem se řídí i závislost rozsahu vazby nízkomolekulárního ligandu na oligomerní vazebnou bílkovinu s kooperujícími podjednotkami (např. vazby kyslíku na hemoglobin). Závislost počáteční reakční rychlosti na koncentraci substrátu u allosterických enzymů (čísla udávají hodnoty koeficientu sigmoidity n) 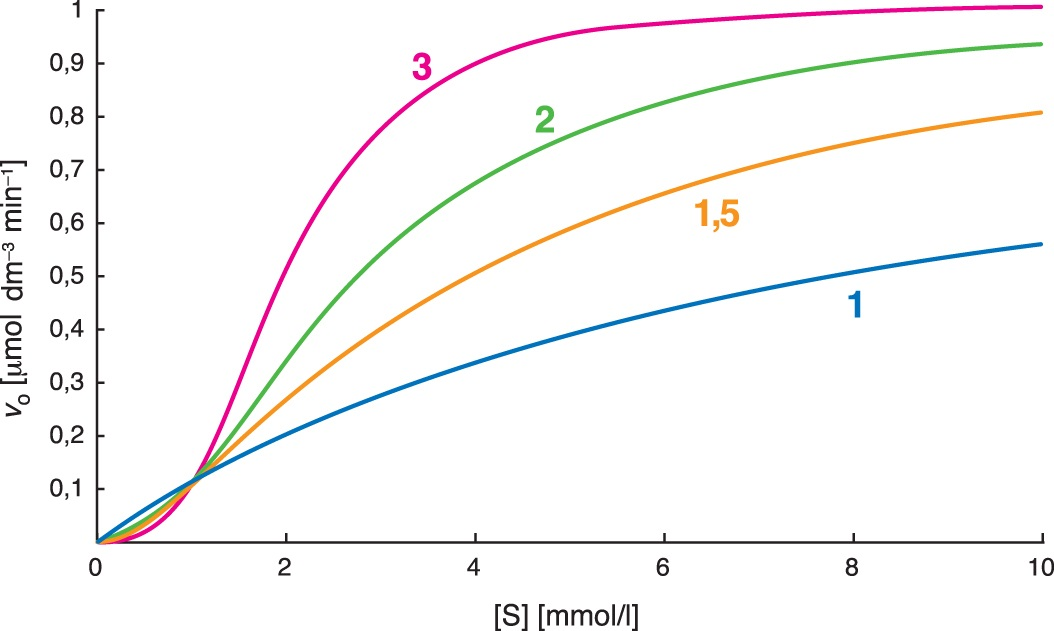 | |
rRNAribosomální
RNA, angl. ribosomal RNA, RNA podílející se spolu se specifickými bílkovinami na výstavbě ribosomu. Je nejhojnějším typem RNA (až 80 hmotn. % všech RNA). Jedná se o několik druhů molekul lišících se velikostí a zastoupením jednotlivých nukleotidů. U eukaryot je syntetizována v jadérku. Vytváří některé specifické sekundární struktury (vlásenky nebo dihelixy podobné DNA). Spolu s ribosomálními proteiny (viz peptidyltransferasa) se podílí na katalýze translace; lze ji tedy považovat za ribozym. | |
RUBISCOribulosa-1,5-bisfosfátkarboxylasa/oxygenasa, angl. též ribulose-1,5-bisphosphate carboxylase/oxygenase, EC 4.1.1.39, enzym ze třídy lyas, který v temné fázi fotosyntézy katalyzuje připojení CO2 k molekule ribulosa-1,5-bisfosfátu a následné rozštěpení vzniklého meziproduktu na dvě molekuly 3-fosfoglycerátu. Kromě této karboxylační reakce (fixace CO2) katalyzuje oxygenační reakci (viz fotorespirace), při níž se na molekulu stejného akceptoru váže molekulový kyslík a kromě 3-fosfoglycerátu vzniká fosfoglykolát. Z něho se sice v rostlinách syntetizuje serin a glycin, většina se však katabolicky odbourává a z hlediska celkové bilance je to ztrátová reakce. 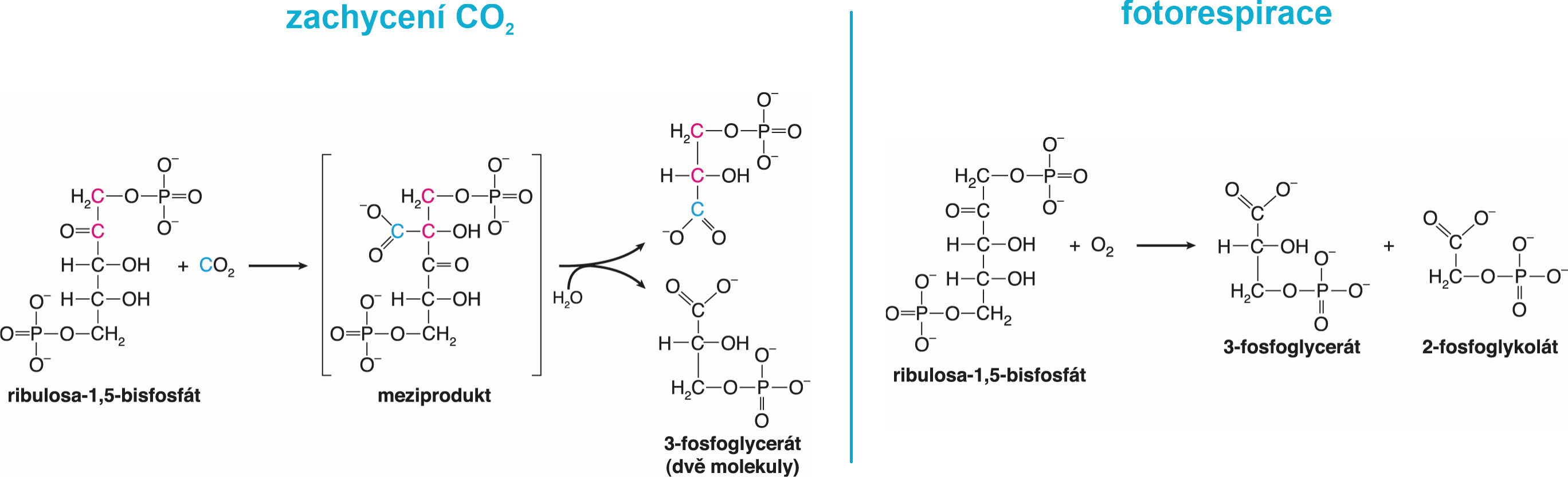 | |
Ružička Leopold
| |
rychlost limitnívlim, nebo maximální vmax , angl. limiting rate nebo velocity, jeden ze základních parametrů rovnice Michaelise a Mentenové (viz enzymy – kinetika), teoreticky nejvyšší počáteční reakční rychlost, jíž může reakce při dané koncentraci enzymu za určitých podmínek (pH, teploty atd.) dosáhnout. Z různých důvodů (inhibice substrátem, omezená rozpustnost substrátů atd.) nemusí být možné této rychlosti experimentálně dosáhnout. | |
rychlost reakční počátečníangl. initial reaction rate nebo initial reaction velocity, pojem užívaný v enzymové kinetice pro rychlost reakce v čase
t = 0, tedy pro rychlost, kterou lze změřit po přidání enzymu do roztoku substrátů. Koncentrace produktů je v tomto okamžiku nulová a reakce tedy probíhá pouze jedním směrem. | |

 chorvatský (rakousko
chorvatský (rakousko