Biochemický slovník
Biochemický slovník
Procházet slovníkem pomocí tohoto rejstříku
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
V |
|---|
vazba anhydridováangl. anhydride bond, vazba mezi dvěma zbytky molekul kyselin. V biochemii jsou zejména významné anhydridové vazby zbytků kyseliny fosforečné (viz difosfát, ATP, ADP, NAD, též směsný anhydrid fosfoadenosinfosfosulfát). | |
vazba disulfidová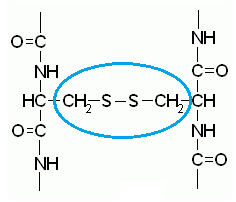 též disulfidový můstek, angl. disulphide bond nebo disulphide bridge, vazba umožňující v bílkovinách kovalentní propojení cysteinových zbytků, a to jak uvnitř jednoho polypeptidového řetězce, tak mezi řetězci; je to významný prvek stabilizace prostorové struktury bílkovin. Disulfidová vazba propojuje i dvě molekuly glutathionu (oxidovaný glutathion). Vzniká oxidací (viz dehydrogenace) dvou thiolových skupin (2 cysteiny → cystin), rozštěpena může být redukcí (in vitro obvykle merkaptoethanolem nebo dithiotreitolem, enzymově s využitím NADPH jako kofaktoru) nebo oxidací (in vitro obvykle peroxomravenčí kyselinou). též disulfidový můstek, angl. disulphide bond nebo disulphide bridge, vazba umožňující v bílkovinách kovalentní propojení cysteinových zbytků, a to jak uvnitř jednoho polypeptidového řetězce, tak mezi řetězci; je to významný prvek stabilizace prostorové struktury bílkovin. Disulfidová vazba propojuje i dvě molekuly glutathionu (oxidovaný glutathion). Vzniká oxidací (viz dehydrogenace) dvou thiolových skupin (2 cysteiny → cystin), rozštěpena může být redukcí (in vitro obvykle merkaptoethanolem nebo dithiotreitolem, enzymově s využitím NADPH jako kofaktoru) nebo oxidací (in vitro obvykle peroxomravenčí kyselinou). | |
vazba fosfodiesterováangl. phosphodiester bond, spojení dvou molekul obsahujících alkoholové skupiny prostřednictvím 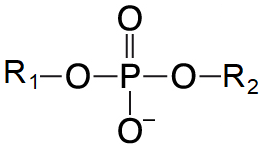 zbytku kyseliny fosforečné, která s nimi vytváří dvě esterové vazby. Tímto způsobem jsou propojeny (deoxy)ribonukleosidy v nukleových kyselinách, diacylglyceroly s polárními alkoholy ve fosfatidátech nebo uhlíky 3′ a 5′ v cyklických nukleosidmonofosfátech (cAMP a cGMP). zbytku kyseliny fosforečné, která s nimi vytváří dvě esterové vazby. Tímto způsobem jsou propojeny (deoxy)ribonukleosidy v nukleových kyselinách, diacylglyceroly s polárními alkoholy ve fosfatidátech nebo uhlíky 3′ a 5′ v cyklických nukleosidmonofosfátech (cAMP a cGMP). | |
vazba glykosidováangl. glycoside bond, propojení monosacharidu s další skupinou prostřednictvím poloacetalového 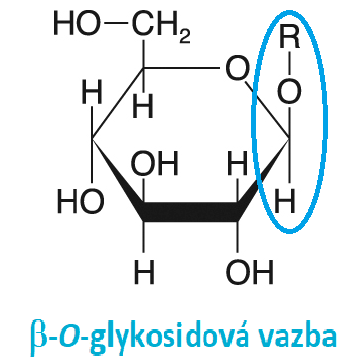 uhlíku. Rozlišujeme vazby O-glykosidové (vazba zprostředkována atomem kyslíku, typické pro oligosacharidy a polysacharidy), N-glykosidové (např. vazba bází na ribosu v nukleosidech, podle názvosloví organické chemie bychom však N-glykosidy měli řadit mezi glykosylaminy) a S-glykosidové. Podle konfigurace na poloacetalovém uhlíku rozlišujeme glykosidové vazby α a β. Pro syntézu glykosidové vazby v živých organismech musí být alespoň jeden z partnerů aktivován (viz např. UDP-glukosa). Její hydrolytické štěpení zajišťují enzymy ze skupiny glykosidas, fosforolytické štěpení pak fosforylasy. uhlíku. Rozlišujeme vazby O-glykosidové (vazba zprostředkována atomem kyslíku, typické pro oligosacharidy a polysacharidy), N-glykosidové (např. vazba bází na ribosu v nukleosidech, podle názvosloví organické chemie bychom však N-glykosidy měli řadit mezi glykosylaminy) a S-glykosidové. Podle konfigurace na poloacetalovém uhlíku rozlišujeme glykosidové vazby α a β. Pro syntézu glykosidové vazby v živých organismech musí být alespoň jeden z partnerů aktivován (viz např. UDP-glukosa). Její hydrolytické štěpení zajišťují enzymy ze skupiny glykosidas, fosforolytické štěpení pak fosforylasy. | |
vazba kooperativníangl. cooperative bond, způsob vazby
ligandu na biopolymer, který má pro něj více vazebných center; typický projev allosterického efektu, při němž jednotlivá vazebná místa kooperují. Při pozitivní kooperativitě první molekula ligandu zvyšuje afinitu biopolymeru k dalším molekulám. Pozitivní kooperativní vazbou váže např. hemoglobin molekuly kyslíku. | |
vazba koordinačně-kovalentnítéž vazba donor-akceptorová nebo koordinační, angl. coordinate covalent bond, dative bond nebo coordinate bond, typ kovalentní vazby
vzniklé tak, že elektrony poskytl jeden z interagujících atomů (donor),
zatímco druhý atom (akceptor) je přijal do svého neobsazeného orbitalu. | |
vazba kovalentníangl. covalent bond, vazba mezi dvěma atomy zprostředkovaná sdílením jednoho, dvou nebo tří párů elektronů, přičemž elektrony jsou poskytovány oběma vazebnými partnery (srov. vazba koordinačně-kovalentní). | |
vazba "makroergická"angl. "macroergic" bond, nešťastné a nepřesné označení vazeb, které se v makroergických sloučeninách štěpí, při čemž se uvolňuje energie. Termín vznikl v době, kdy panoval názor, že veškerá energie, která se při štěpení takovéto vazby uvolní, je lokalizována výhradně v ní; později se ukázalo, že zejména u nukleosidtrifosfátů (ATP, GTP) tomu tak není. | |
vazba peptidováangl. peptide bond, vazba mezi dvěma molekulami aminokyselin (resp. mezi dvěma aminokyselinovými zbytky), zvláštní typ sekundární amidové vazby. Vzhledem k velké 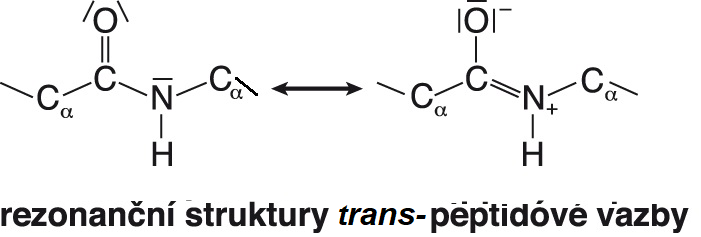 elektronegativitě atomu kyslíku se volný elektronový pár na dusíkovém atomu přesunuje a vazba CO–NH získává částečně dvojný charakter; v bílkovinách a přirozených peptidech převažuje uspořádání trans, pouze peptidová vazba vycházející z iminokyseliny prolinu bývá v uspořádání cis. Peptidová vazba je i ve vodném prostředí stálá. Hydrolyzuje při zvýšené teplotě v prostředí silné kyseliny nebo zásady; její hydrolýzu v organismech katalyzuje velké množství enzymů ze skupiny peptidas. Pro její syntézu ve vodném prostředí je zapotřebí nejdříve aktivovat karboxylovou skupinu reagující aminokyseliny; pro chemickou syntézu (in vitro) byly vypracovány různé způsoby této aktivace, při biosyntéze se aminokyselina obvykle aktivuje vazbou na příslušnou tRNA. 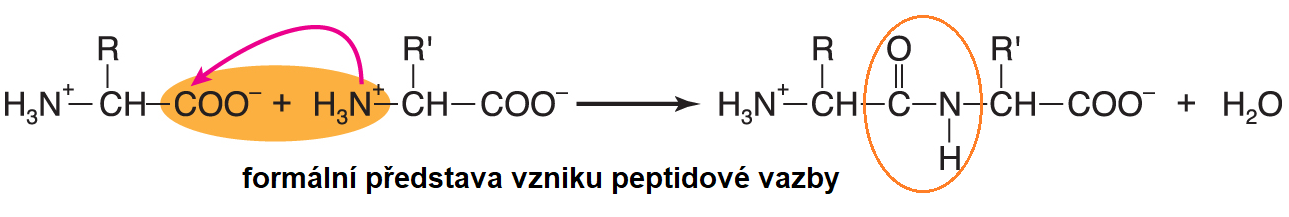 | |
vazba thioesterováangl. thioester bond, vazba zbytku karboxylové kyseliny a thiolu; významné jsou zejména thioestery karboxylových kyselin vázaných na 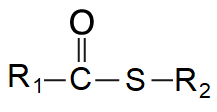 koenzym A (acyl-CoA) a z nich zejména acetyl-CoA; označují se také jako acyl-SCoA nebo acetyl-SCoA . koenzym A (acyl-CoA) a z nich zejména acetyl-CoA; označují se také jako acyl-SCoA nebo acetyl-SCoA . | |
