Biochemický slovník
Biochemický slovník
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
D |
|---|
Dam Henrik Carl Peter
| |
David Baker
| |
deaminaceangl. deamination, odstranění aminoskupiny z molekuly, v biochemii nejčastěji hydrolyticky (např. deaminace adeninu, také deamidace
glutaminu a asparaginu), lyasovou reakcí (deaminace aspartátu na fumarát) nebo oxidačně (viz oxidační deaminace). | |
deaminace oxidačníangl. oxidative deamination, reakce, při níž je z aminokyselin odstraňován dusík a vzniká 2-oxokyselina. Nejdříve se aminoskupina dehydrogenuje: 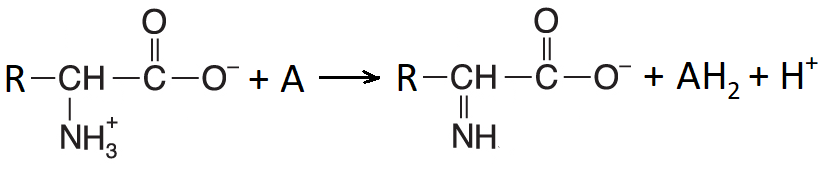 přičemž akceptorem vodíku (A) může být molekulový kyslík (vzniká H2O2, oxidasy aminokyselin s prostetickou skupinou FMN, EC 1.4.3.-) nebo NAD(P)+ (viz glutamátdehydrogenasa, EC 1.4.1.-). Vzniklá iminokyselina se následně (za katalýzy stejným enzymem) hydrolyticky rozkládá na příslušnou 2-oxokyselinu a amoniak: 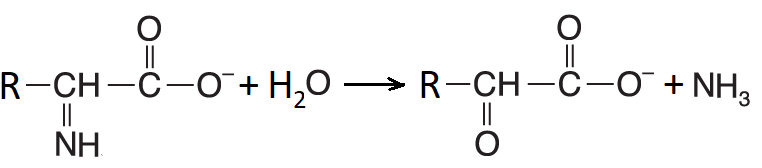 | |
degenerace genetického kóduangl. genetic code degeneration, pojem, indikující, že pro jednu proteinogenní aminokyselinu existuje více kodonů. Poznámka: Podobně říkáme, že určité atomové nebo molekulové orbitaly jsou degenerované, jestliže mají stejnou energii; nejznámějším příkladem jsou sp3 hybridizované orbitaly uhlíku v nasycených uhlovodících, ale i pětice orbitalů d v izolovaných atomech přechodných kovů. | |
dehydrataceangl. dehydration nebo dehydratation,
| |
dehydrogenaceangl. dehydrogenation, odštěpování vodíku (obvykle dvou atomů) ze
substrátu. Proces katalyzovaný enzymy ze třídy oxidoreduktas (nazývají se proto dehydrogenasy). Akceptorem vodíku jsou nejčastěji pyridinové koenzymy NAD(P) (např. 3 dehydrogenasy v citrátovém cyklu), může jím však být i jiný koenzym oxidoreduktas, např. ubichinon (sukcinátdehydrogenasa citrátového cyklu, EC 1.3.5.1). Přenos atomů vodíku na molekulový kyslík katalyzují oxidasy; tento typ reakce se mezi dehydrogenace obvykle nezařazuje. | |
dekarboxylaceangl. decarboxylation, odštěpování oxidu uhličitého ze
substrátu, proces katalyzovaný enzymy ze třídy lyas nebo oxidoreduktas (viz oxidační dekarboxylace). K nejznámějším (neoxidačním) dekarboxylasám patří pyruvátdekarboxylasa (EC 4.1.1.1), produkující acetaldehyd při alkoholové fermentaci, či dekarboxylasy aminokyselin (EC 4.1.1.11 a další), jejichž působením vznikají biogenní aminy. | |
dekarboxylace oxidačníangl. oxidative decarboxylation, dekarboxylace, při níž dochází k odštěpení CO2 následkem předchozí oxidace (resp. dehydrogenace) substrátu; je katalyzována enzymy ze třídy oxidoreduktas. Tak z citrátového cyklu známe isocitrátdehydrogenasu (EC 1.1.1.41) katalyzující vznik 2-oxoglutarátu, a multienzymovou jednotku, která přeměňuje 2-oxoglutarát na sukcinyl-CoA; podobná jednotka přeměňuje pyruvát na acetyl-CoA (pyruvátdehydrogenasový komplex). V pentosovém cyklu oxidačně dekarboxyluje 6-fosfoglukonát na ribulosa-5-fosfát (fosfoglukonátdehydrogenasa, EC 1.1.1.44). Z pyruvát-malátového cyklu a z metabolismu C4-rostlin známe "jablečný enzym" (EC 1.1.1.40), který oxidačně dekarboxyluje malát na pyruvát za současné redukce NADP+. | |

 (nar. 1962), americký biochemik a počítačový biolog, Nobelova cena (za chemii, 2024) za počítačové navrhování proteinů (spolu s J. M. Jumperem a D. Hassabisem). Narodil se v židovské rodině v Seattlu, jeho otec byl fyzik a matka geofyzička. Vystudoval filozofii a společenské vědy, pak se však začal věnovat biochemii a proteinovým strukturám. V roce 1989 získal doktorát z biochemie; zabýval se převážně proteiny v kvasinkách. Od roku 1993 vede vlastní výzkumnou skupinu na lékařské fakultě Washingtonské univerzity, kde působí také jako pedagog. Počítačové programy umělé inteligence, vyvinuté Bakerem a jeho skupinou, jsou klíčové v oblasti předpovídání struktury proteinů. V roce 2003 se jim podařilo navrhnout zcela nový protein. Od té doby navrhuje i další proteiny, včetně takových, které lze použít jako
(nar. 1962), americký biochemik a počítačový biolog, Nobelova cena (za chemii, 2024) za počítačové navrhování proteinů (spolu s J. M. Jumperem a D. Hassabisem). Narodil se v židovské rodině v Seattlu, jeho otec byl fyzik a matka geofyzička. Vystudoval filozofii a společenské vědy, pak se však začal věnovat biochemii a proteinovým strukturám. V roce 1989 získal doktorát z biochemie; zabýval se převážně proteiny v kvasinkách. Od roku 1993 vede vlastní výzkumnou skupinu na lékařské fakultě Washingtonské univerzity, kde působí také jako pedagog. Počítačové programy umělé inteligence, vyvinuté Bakerem a jeho skupinou, jsou klíčové v oblasti předpovídání struktury proteinů. V roce 2003 se jim podařilo navrhnout zcela nový protein. Od té doby navrhuje i další proteiny, včetně takových, které lze použít jako