Biochemický slovník
Biochemický slovník
Procházet slovníkem pomocí tohoto rejstříku
Speciální | A | Á | B | C | Č | D | Ď | E | É | Ě | F | G | H | CH | I | Í | J | K | L | M | N | Ň | O | Ó | P | Q | R | Ř | S | Š | T | Ť | U | Ú | Ů | V | W | X | Y | Ý | Z | Ž | VŠE
A |
|---|
alkalózaangl. alkalosis, patologický stav, při němž pH krve po delší dobu překračuje hodnotu 7,45 (srov. acidóza). | |
alkoholdehydrogenasaangl. alcohol degydrogenase, zkr. ADH (EC 1.1.1.1), velmi rozšířený enzym ze třídy
oxidoreduktas; metaloenzym obsahující Zn2+. Katalyzuje reakci primární alkohol + NAD+ 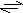 aldehyd + NADH + H+. Jaterní alkoholdehydrogenasa odbourává ethanol produkovaný střevní mikroflorou, ale také ethanol přijatý z vnějších zdrojů; v případě dědičného sklonu k alkoholismu bývá její aktivita snížena. Při alkoholové fermentaci redukuje acetaldehyd na ethanol a regeneruje tak NAD+, potřebný v glykolyse. Substrátová specifita některých isoenzymů je široká a jsou schopné katalyzovat i oxidaci methanolu na formaldehyd, což je příčinou vážných důsledků otravy methanolem. aldehyd + NADH + H+. Jaterní alkoholdehydrogenasa odbourává ethanol produkovaný střevní mikroflorou, ale také ethanol přijatý z vnějších zdrojů; v případě dědičného sklonu k alkoholismu bývá její aktivita snížena. Při alkoholové fermentaci redukuje acetaldehyd na ethanol a regeneruje tak NAD+, potřebný v glykolyse. Substrátová specifita některých isoenzymů je široká a jsou schopné katalyzovat i oxidaci methanolu na formaldehyd, což je příčinou vážných důsledků otravy methanolem. | |
allosterieangl. allostery, jev, při němž je konformační změna určité části molekuly bílkoviny vyvolána konformační změnou v jiné části molekuly (viz allosterický efekt). | |
Altman Sidney
| |
amfiontytéž amfoterní ionty nebo amfolyty, angl. amphions / zwitterions, částice, obsahující jak kyselé, tak bazické skupiny. Typickými představiteli amfiontů jsou
aminokyseliny; v neutrálním roztoku jejich karboxylová skupina ztrácí proton a vzniká z ní záporně nabitá skupina -COO-, aminoskupina zde proton přijímá za vzniku -NH3+. Volný náboj aminokyseliny, obsahující jednu karboxylovou a jednu aminovou skupinu, je tedy v neutrálním roztoku nulový. Pro každý amfion existuje určitá hodnota pH, při níž má nulový volný náboj (isoelektrický bod). | |
amidasyangl. amidases, EC 3.5.1.-, hydrolasy, štěpící vazbu C-N v lineárních amidech: R-CONH2 + H2O → R-COO- + NH4+; do této skupiny však nepatří peptidasy. Acylamidamidohydrolasa (EC 3.5.1.4) katalyzuje hydrolýzu amidů bez substrátové specifity, ostatní jsou specifické pro jednotlivé amidy, např. asparaginamidohydrolasa (EC 3.5.1.1), glutaminamidohydrolasa (EC 3.5.1.2) či ureasa (EC 3.5.1.5). | |
aminoacyl-tRNA-ligasytéž aminoacyl-tRNA-synthetasy, angl. aminoacyl-tRNA ligases, EC 6.1.1.1 - EC 6.1.1.22, enzymy katalyzující reakci: aminokyselina + tRNA + ATP→ aminoacyl-tRNA + AMP + PPi. Jde o přípravuaminokyselin pro vstup do biosyntézy bílkovin (translace): aminokyselina se vazbou na tRNA aktivuje a současně označuje (antikodonem tRNA) tak, aby mohla být správně zařazena do rostoucího peptidového řetězce. Tyto ligasy jsou specifické pro jednotlivé dvojice aminokyselina - tRNA. | |
aminocukryangl. amino sugars, monosacharidy, jejichž jedna hydroxylová skupina je nahrazena skupinou aminovou. Významné jsou zejména 2-deoxy-2-aminoaldosy a jejich N-acetylované deriváty (N-acetylglukosamin, N-acetylgalaktosamin, neuraminová kyselina atd.), které tvoří běžné složky glykoproteinů, extracelulárních polysacharidů (hmyzí chitin, hyaluronová kyselina v chrupavkách, polysacharidy bakteriálních buněčných stěn) i oligosacharidů vyskytujících se v mléce. Systémově vzato, jedná se o deriváty deoxycukrů (vzorce viz tamtéž). | |
aminokyselinyangl. amino acids, aminokarboxylové kyseliny, substituční deriváty karboxylových kyselin, které obsahují v uhlíkovém řetězci aminoskupinu; biologicky nejvýznamnější aminokyseliny obsahují tuto skupinu v poloze α (jsou to tedy 2-aminokarboxylové kyseliny). Volné aminokyseliny existují ve formě
amfiontů. Aminokyseliny jsou základními stavebními jednotkami peptidů a bílkovin, v nichž jsou sousedící zbytky spojeny peptidovou vazbou. V biochemii dělíme aminokyseliny podle různých hledisek: na aminokyseliny proteinogenní a neproteinogenní, esenciální a neesenciální, ketogenní a glukogenní. | |
aminokyseliny esenciální a neesenciálníangl. essential and non-essential amino acids, rozdělení
proteinogenních aminokyselin podle toho, zda si je heterotrofní organismus dokáže sám syntetizovat, nebo zda je musí přijímat potravou. Pro člověka jsou esenciální aminokyseliny Val, Leu, Ile, Phe, Trp, His, Lys, Met a Thr, u novorozenců je kritický též Arg. Ostatní proteinogenní aminokyseliny nazýváme neesenciální. Poněkud problematické je zařazení aminokyseliny Tyr, která vzniká modifikací esenciálního Phe, a aminokyseliny Cys vznikajícího z Met; tyto aminokyseliny bývají někdy nazývány podmíněně esenciální. Uhlíková kostra ostatních neesenciálních aminokyselin vzniká z běžných metabolitů (pyruvátu, oxalacetátu, 2-oxoglutarátu či 3-fosfoglycerátu). | |

